Дробление - вещество
Cтраница 2
Работа, затраченная при дроблении вещества на разрыв связей между молекулами, превращается в потенциальную энергию ненасыщенных связей на границах раздела фаз. В связи с увеличением ( во много раз) поверхности раздела в процессе диспергирования вещества эта избыточная поверхностная энергия достигает значительной величины. Обладая в мелкодисперсном состоянии большей энергией, вещество, следовательно, обладает и большей активностью, нежели неизмельченное. [16]
Таким образом, при дроблении вещества быстро растет удельная поверхность. Совершенно очевидно, что в такой же степени растет и свободная поверхностная энергия. При значительном раздроблении вещества поверхностная энергия - начинает играть значительную и даже решающую роль. Из приведенной таблицы видно, что удельная поверхность достигает громадных цифр при той степени раздробленности, которой характеризуются коллоиды. Естественно, что в коллоидных системах в связи с этим имеется огромная поверхностная энергия. [17]
 |
Схема коллоидной мельницы. [18] |
Более высокая дисперсность получается при дроблении веществ в коллоидной мельнице. В результате быстрого вращения вала кусочки предварительно измельченного вещества, загружаемого вместе с жидкостью и стабилизатором в мельницу ( с), ударяются с большой силой о выступы и лопасти, разбиваясь при этом на мелкие частицы. [19]
 |
Шаровая мельница. [20] |
В этих методах диспергирование осуществляется путем дробления вещества с помощью мельниц различных типов. Чаще всего используют шаровые мельницы. [21]
Только что указанные способы основаны на дроблении вещества и являются, таким образом, дисперсионными способами. [22]
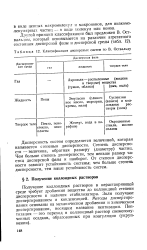 |
Классификация дисперсных систем по В. Оствальду. [23] |
Получение коллоидных растворов в нерастворяющей среде требует дробления вещества до коллоидной степени дисперсности и наличия стабилизатора. Золи получают диспергированием и конденсацией. Методы диспергирования основаны на механическом дроблении и химическом диспергировании, носящим название пептизации. [24]
При более высоких температурах быстрое образование продукта вызывает дробление вещества и реакция идет с ускорением до больших глубин разложения, в то время как при низких температурах вокруг микрозерен образуются сокращающиеся оболочки продукта. [25]
Коллоидные растворы можно получить: 1) путем дробления вещества до размеров коллоидных частиц; 2) создавая условия, при которых молекулы соединяются в более крупные частицы, однако по размерам не превосходящие коллоидных частиц. Способы первого рода называются дисперсионными, способы второго рода - конденсационными. [26]
В табл. 43 для иллюстрации приводится изменение суммарной поверхности по мере дробления вещества. [27]
Верхний предел дисперсности коллоидных систем обусловлен тем, что при даль - нейшем дроблении вещества в растворе уже будут находиться не агрегаты молекул, а отдельные молекулы, имеющие размер порядка 0 1 нм. Нижний предел дисперсности коллоидных систем определяется резким снижением интенсивности теплового движения частиц поперечным размером больше 100 нм. Несмотря на установленный предел в 100 нм в курсе коллоидной химии рассматриваются обычно и более грубодисперсные системы, размер частиц которых может достигать несколько микрометров, а иногда и значительно больше. [28]
Для решения сформулированных задач оптимизации необходимо иметь математические модели дробильных агрегатов, отражающие физические и энергетические составляющие процесса дробления вещества. [29]
В предыдущих разделах мы рассматривали первый из двух основных способов образования аэрозолей - дисперсионный, при котором мелкие частицы образуются путем дробления вещества. Обратимся теперь ко второму из этих способов - конденсационному, при котором мельчайшие частицы образуются путем конденсации паров. [30]
Страницы: 1 2 3 4