Мембрана - электрод
Cтраница 3
Наиболее простыми и логически обоснованными представляются такие названия электродов, для которых потенциалопреде-ляющий и аналитически определяемый ион совпадают. Например, если определяемым ионом является катион меди ( II), а мембрана электрода содержит сульфид меди ( II) и потенциал-определяющим ионом в этом случае также является катион ме-ди ( П), то такой электрод правильнее всего назвать медь ( П) - се-лективным, или, если указывать степень окисления нет необходимости, просто медь-селективным электродом. Это правило распространяется на все электроды, для которых справедливо требование о совпадении химической формы потенциалопределяю-щей и аналитически определяемой частицы. [31]
Такое разделение не может считаться достаточно строгим, так как многие растворители способны в од них случаях преимущественно сольватировать катионы, в других - анионы. Таким образом, следует отметить принципиальную важность выбора растворителя для жидкой ( или пленочной) мембраны электрода. Растворитель может существенно изменить селективные свойства мембраны. Можно сказать, что инертных растворителей не существует. Степень влияния их на свойства мембраны определяется их соль-ватирующей способностью. [32]
 |
Прибор для сжигания с последующим титрованием ( г. [33] |
Гранулированный кварцевый песок располагают с обеих сторон от платинированной кварцевой ваты, как это показано на рис. 6.3. Трубку 3 нагревают в печи 70 до 1000 С. Титрант добавляется из бюретки через полиэтиленовый капилляр, кончик которого располагается в трубке 8 несколько ниже поверхности мембраны электрода. Поршень шприца сделан из нержавеющей стали, а его наконечник - из тефлона, рукоятка - из алюминия. Платиновая игла закреплена в капилляре эпоксидной смолой. [34]
Для технологических растворов длительность достижения равновесия увеличивается из-за сорбции ионов различных зарядов и образования на поверхности раздела фаз мембраны электрода стационарного слоя, замедляющего скорость ионного обмена. [35]
Кристалл нерастворимой в воде соли является ионопроводящей фазой, если один из двух составляющих его ионов способен перемещаться по дефектам в кристаллической решетке под действием электрического поля. Пластинка такого, монокристалла может быть мембраной электрода, специфичного к одному из ионов соли. Специфичность кристаллического электрода определяется произведением растворимости соли, образующей кристалл. [36]
В этом случае анализируемую пробу подкисляют 3 - 4 каплями 70 % - ной хлорной кислоты, чтобы удалить фтор в виде фтористого водорода. Из-за того что фосфат образует нерастворимую соль со свинцом, фосфат-ионы мешают определению сульфата. Вследствие того что Ag и Fe3 разрушают мембрану электрода, эти методы непригодны для отделения фосфата. [37]
Измерение потенциала растворов проводят на рН - метре или иономере согласно инструкции к прибору, начиная с самого разбавленного раствора и используя в качестве измерительного электрода фторселективный, а в качестве электрода сравнения - хлорсеребряный. Исследуемый раствор наливают в химический стакан и помещают на включенную магнитную мешалку, опускают в него электроды и через 5 мин снимают показания прибора. После каждого измерения электроды промывают дистиллированной водой и осторожно осушают фильтровальной бумагой, стараясь не повредить мембрану ионселек-тивного электрода. [38]
В этом дополнении к монографии рассматриваются только такие случаи, когда между стеклом и раствором распределяются лишь однозарядные ионы. В литературе обсуждаются и более сложные случаи распределения между рассматриваемыми фазами ионов разного по величине заряда. Недавно получены новые выражения для потенциала ионообменного электрода, в которых учитываются как межфазные разности потенциала, так и диффузионный потенциал внутри мембраны электрода для такого случая, когда между ионообменной мембраной и раствором распределяются одно - и двухзарядные ионы. [39]
В этом дополнении к монографии рассматриваются только такие случаи, когда между стеклом и раствором распределяются лишь однозарядные ионы. В литературе обсуждаются и более сложные случаи распределения между рассматриваемыми фазами ионов разного по величине заряда. Недавно получены новые выражения для потенциала ионообменного электрода, в которых учитываются как мвжфазные разности потенциала, так и диффузионный потенциал внутри мембраны электрода для такого случая, когда между ионообменной мембраной и раствором распределяются одно - и двухзарядные ионы. [40]
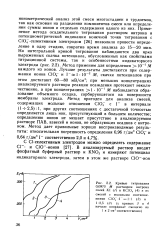
Lgtf KCl для поликристаллических хло-ридных мембран с различным содержанием AjfcS представлены на рис. 1 а. В растворе С концентрацией I-IO m KC1 имеют место небольшие отклонения от теоретической функции. При исследовании воспроизводимости электродных потенциалов во времени было обнаружено, что с течением времени ( через 2 - 3 недели) наблюдается незначительное уменьшение величины углового коэффициента калибровочных кривых, которое, очевидно, связано с загрязнением поверхности мембраны электрода. Полировка рабочей поверхности мембраны возвращает электроду его прежние характеристики. [41]
Применение метода осадительного титрования раствором нитрона и потенциометрической индикации конечной точки титрования с СЮ - селективным электродом [26] позволило провести определение в одну стадию, сократив время анализа до 15 - 20 мин. Метод применим для определения 10 - 3 М каждого из ионов. Лучшие результаты достигаются при содержании ионов C1CV и 1 - - 1 - 10 - 2 М, скачки потенциалов при этом достигают 60 - 80 мВ / см3; при меньших концентрациях анализируемого раствора реакции осаждения протекают неколичественно, а при концентрациях 1 10 - М наблюдается образование объемного осадка, сорбирующегося на поверхности мембраны электрода. Метод пригоден для анализа смесей, содержащих мольные отношения С1ОГ с 1 - в интервале ( 1ч - 2 5): 1, при других соотношениях с достаточной точностью определяется лишь ион, присутствующий в большем количестве; определению ионов не мешает присутствие в анализируемом растворе ПАВ, взвесей и ионов, не образующих осадков с нитроном. [43]
В этой главе мы рассмотрим свойства ионоселек-тивных электродов, мембраны которых представляют собой моно - или поликристаллы труднорастворимых в воде солей. В этих мембранах обычно один из двух составляющих соль ионов способен под действием электрического поля перемещаться в кристаллической решетке по ее дефектам. Примерами кристаллических электродов могут служить в первую очередь системы с мембранами из солей галогенидов серебра, которые, как известно, обладают ионной проводимостью, осуществляемой ионами серебра. Тонкая пластинка из монокристалла, например, хлорида серебра, может быть мембраной электрода, обратимой по отношению к иону С1 -, который закреплен в кристаллической решетке. [44]
Выпущен электрод модели 94 - 09 А с мембраной из монокристалла LaF3) укрепленной в конце пластмассовой трубки. По конструкции электрод подобен стеклянному электроду, только вместо стеклянной мембраны в нем использована мембрана из монокристалла фторида лантана, легированного европием. Так же как с помощью стеклянного электрода измеряют активность ионов водорода, фторидным электродом измеряют активность ионов фторида. В обоих электродах измеряют разность потенциалов двух поверхностей тонкой мембраны, характеризующейся ионной проводимостью, но в отличие от стеклянного электрода мембрану фто-ридного электрода не обязательно выдерживать в воде перед использованием. Потенциал Ag / AgCl-электрода определяется активностью хлорид-ионов во внутреннем растворе, активность фторид-ионов в том же растворе определяет потенциал внутренней поверхности кристаллической мембраны фторида лантана. [45]
Страницы: 1 2 3