Мера - реакция
Cтраница 3
В первой из указанных систем образцовым приемником является средний глаз человека, во второй мерой реакции на излучение принята некоторая средняя характеристика губительного действия ультрафиолетового излучения на бактерии, в третьей - покраснение кожи человека и последующая пигментация ее в результате облучения. Из этих трех систем одна предназначена для оценки эффективности излучения видимого участка спектра, а две - для ультрафиолетового излучения. [31]
Поскольку р / С - нитрофенола составляет 7 5, то неясно, в какой мере реакции ( 57) и ( 63) определяются - нитрофенолят-ионами или протониро-ванной формой - нитрофенола. [32]
Это определение позволяет сделать вывод, существенно важный для светотехнической практики: равным эффективным потокам соответствует равная мера реакции приемника. [33]
Таким образом, для каждой конкретной реакции может быть получено выражение, связывающее константу равновесия с мерой реакции ( степенью превращения, степенью диссоциации) и объемом или давлением. Эти выражения дают возможность оценить влияние объема и давления на положение равновесия, а также определить меру реакции ( степень превращения, степень диссоциации), если известна константа равновесия ( или наоборот), и следовательно, равновесный состав смеси. Знание равновесного состава смеси очень важно для практики. Так же важно установление влияния давления и объема на положение равновесия. [34]
Таким образом, для каждой конкретной реакции может быть получено выражение, связывающее константу равновесия с мерой реакции ( степенью превращения, степенью диссоциации) и объемом или давлением. Эти выражения дают возможность оценить влияние объема и давления на положение равновесия, а также определить меру реакции ( степень превращения, степень диссоциации), если известны константа равновесия ( или наоборот) и, следовательно, равновесный состав смеси. Знание равновесного состава смеси очень важно для практики. Так же важно установление влияния давления и объема на по - ложен не равновесия. [35]
Если препарат В2 содержит лишь индикаторные количества препарата BI, то степень превращения Х2 можно рассматривать как меру макроскопической реакции. [36]
Это значит, что табличное значение теплового эффекта представляет собой тепловой эффект химической реакции, отнесенный к мере реакции Д, при условии, что мера реакции численно равна изменению числа кило-молей вещества An, на 1 кмоль которого дается тепловой эффект. Следует обратить внимание на то, что часто в термохимии для количества теплоты принимают противоположное правило знаков по сравнению с принятым в технической термодинамике, а именно, теплота, подведенная к системе, рассматривается как отрицательная, а отведенная, как положительная. [37]
Уравнение ( 22) дает возможность выразить число молей каждого из веществ в системе по окончании реакции через меру реакции. [38]
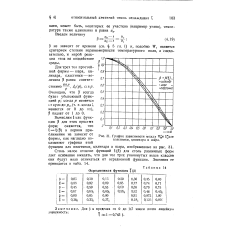 |
Осредненная функция f ( Ю. [39] |
I) и, подобно Т, является критерием степени неравномерности температурного поля, а следовательно, и мерой реакции тела на воздействие среды. [40]
И хотя альдегидной формы в равновесии содержится совсем мало, все же вся глюкоза подвергается окислению, так как по мере реакции циклическая форма переходит в альдегидную и пополняет ее запасы. [41]
АТР - соответственно количество теплоты и максимальная немеханическая работа в равновесном процессе при Т, р - const, отнесенные к мере реакции. Если процесс перераспределения массы необратимый, то немеханическая работа превратится в теплоту и количество теплоты в этом случае будет равно изменению энтальпии, Л / г, сложной системы. [42]
АТр - соответственно количество теплоты и максимальное количество немеханической работы в равновесном процессе при Т, р const, отнесенные к мере реакции. Если процесс перераспределения массы необратимый, то немеханическая работа превратится в теплоту и количество теплоты в этом случае будет равно изменению энтальпии АЯГр сложной системы. [43]
Поэтому для ионов р-злементов характерны реакции окисления-восстановления ( только алюминий имеет одну степень окисг ления А1 ( Ш) -) и в некоторой мере реакции комплексообразо-вания. [44]
Это значит, что табличное значение теплового эффекта представляет собой тепловой эффект химической реакции, отнесенный к мере реакции Д, при условии, что мера реакции численно равна изменению числа кило-молей вещества An, на 1 кмоль которого дается тепловой эффект. Следует обратить внимание на то, что часто в термохимии для количества теплоты принимают противоположное правило знаков по сравнению с принятым в технической термодинамике, а именно, теплота, подведенная к системе, рассматривается как отрицательная, а отведенная, как положительная. [45]
Страницы: 1 2 3 4