Баланс - вещество
Cтраница 1
Баланс веществ, участвующих в окислительно-восстановительных процессах, определяется количеством электронов, теряемых частицей восстановителя и присоединяемых частицей окислителя. При этом степени окисления элементов изменяются в соответствии с числом потерянных ( или присоединенных) атомом электронов. Поэтому эквивалентные массы окислителя и восстановителя зависят от изменения в результате реакции степеней окисления элементов, входящих в эти вещества, что учитывается фактором эквивалентности. [1]
Баланс веществ, участвующих в окислительно-восстановительных процессах, определяется числом электронов, теряемых частицей восстановителя и присоединяемых частицей окислителя. При этом степени окисления элементов изменяются в соответствии с числом потерянных ( или присоединенных) атомом электронов. Поэтому эквивалентные массы окислителя и восстановителя зависят от изменения в результате реакции степеней окисления элементов, входящих в эти вещества, что учитывается фактором эквивалентности. [2]
Баланс вещества в слое Нернста определяется миграцией и диффузией ионов без перемешивания с массой. Избирательный перенос одного из ионов вызывает таким образом уменьшение количества этого иона в слое Нернста, мембрана уравновешивается с раствором, который содержит меньшее количество избирательных ионов по сравнению с исходным раствором. [3]
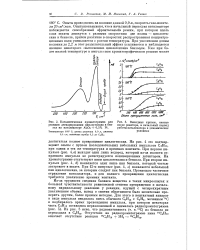
Рассмотрим баланс вещества при протекании реакции в цилиндрической поре радиусом R и длиной L. [4]
 |
К выводу уравнения баланса веществ. [5] |
Рассмотрим баланс вещества г - го компонента. Входящее количество вещества в элементарный объем через грань dydz за время dt будет равно u nidydzdt, где HI - концентрация z - ro компонента на входе в элементарный объем. [6]
Уравнение баланса веществ вытекает из закона сохранения вещества. [7]
Уравнение баланса вещества ( 21) записано в координатах Ла-гранжа. [8]
Система уравнений баланса вещества и кинетики сорбции при дополнительных условиях ( буферный объем нагнетаемого раствора задается в виде граничного условия в начальный промежуток времени, на контуре пласта и в начальный момент времени в пласте нулевая концентрация раствора) при постоянном коэффициенте кинетики сорбции и изотерме Генри заменой переменных приводится к задаче одномерного движения. Дальнейшее решение системы уравнений получено в виде сходящегося ряда преобразованием Лапласа. Построены графики пространственно-временного распределения ПАВ. С помощью полученного решения и экспериментальной зависимости коэффициента использования емкости пласта от концентрации раствора построена зависимость объема газохранилища с одиночной скважиной от начального объема и концентрации нагнетаемого раствора. Приводится сравнение объема хранилища при использовании ПАВ и без них. [9]
Составим уравнение баланса вещества в активной и пассивной фазах для двух крайних гидродинамических режимов - идеального вытеснения и идеального смешения. [10]
Кажущиеся нарушения баланса вещества и закона Фарадея могут быть связаны и с протеканием процесса, не являющегося фарадеевским. Поэтому вес перешедших в раствор ионов титана точно соответствует закону Фарадея, однако он значительно меньше, чем убыль веса электрода, лишь частично связанная с фарадеевским растворением титана. [11]
Составим уравнение баланса вещества с учетом этого обстоятельства. [12]
Общие вопросы составления баланса вещества в химической реакции освещаются во многих книгах, в том числе в большей части монографий, указанных в библиографии к главе I. [13]
Из-за трудности сведения баланса вещества в таких микроопытах и большой чувствительности равновесной степени превращения к начальному парциальному давлению у реакции, идущей с четырехкратным увеличением объема, вывод о снятии обратимости было желательно проверить другим, более прямым методом. [15]
Страницы: 1 2 3 4