Фазовая диаграмма - система
Cтраница 4
В приложение включены тройные и многокомпонентные полярные фазовые диаграммы систем, представляющие интерес с точки зрения химического состава суперсплавов ( рис. А. Для экономии места диаграмма системы Ni-Fe-Co, обладающей в представляющей интерес области полной взаимной растворимостью, не приведена. [46]
Последнее означает изменение фазовой диаграммы системы под влиянием поверхности наполнителя. При этом особый интерес представляют особенности фазового разделения внутри спинодали. [47]
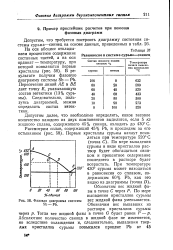 |
Равновесие в системе сурьма-свинец.| Фазовая диаграмма системы вес жидкой фазы уменьшается. [48] |
В результате получим фазовую диаграмму системы Sb - РЬ. [49]
 |
Фазовая диаграмма растворов ПАВ вблизи точки Крафта. [50] |
По аналогии с фазовой диаграммой системы лед - вода можно предположить, что при возрастании температуры разница между концентрацией переохлажденных мицелл и гидратированного твердого ПАВ уменьшается. Выше точки Крафта равновесная концентрация мицелл становится меньше, чем концентрация ( гипотетического) перегретого гидратированного твердого ПАВ, и поэтому мицеллы являются термодинамически более выгодной формой. С повышением температуры по достижении определенной точки наблюдается быстрое возрастание общей растворимости. Это явление связано с постоянством активности растворенного вещества выше ККМ. [51]
На рис. 75 показана фазовая диаграмма системы хлорид натрия - вода. Например, если охлаждается раствор хлорида натрия, имеющий начальную концентрацию NaCl 5 % и температуру около 10 ( точка /), то при температуре t - 2 85 ( пересечение линий АС и I s) начинает выделяться чистый лед. При этой температуре полностью затвердевшая смесь содержит лед и эвтектическую смесь, в состав которой входит 23 % соли и 77 % воды. Если же раствор хлорида натрия имеет начальную концентрацию NaCl 26 % и температуру 75, то при охлаждении сначала выпадает в осадок только соль до достижения температуры - 21 2, когда затвердевает и эвтектическая смесь. [52]
 |
Смещение фазовой диаграммы давление-состав под действием капиллярных сил. [53] |
При отсутствии капиллярных сил фазовая диаграмма системы изображается на рисунке кривой AKRA. На этой кривой / С - критическая точка, Л - давление пара чистого менее летучего компонента 2, АК - кривая точек давления насыщения, KRA - кривая точек росы. [54]
На рис. 10.2 показана фазовая диаграмма системы о-броманилин - пикриновая кислота, на которой обнаруживается ряд интересных особенностей. [55]
На рис. 2 приведена фазовая диаграмма двухком-понентной системы, состоящей из растворителя и полимера с молекулярным весом порядка 50000 и значением мольного объема около 10 - 3 м3 / моль. [56]
В работе [1] приведены фазовые диаграммы систем МО-X Os, отражающие наиболее вероятные фазовые равновесия и термические характеристики ванадатов магния, кальция, стронция и бария. Ванадат Ca7V4Oi7 выше 1100 С разлагается на ортованадат и оксид кальция. Температура конгруэнтного плавления ванадата кальция состава Ca A / sOg равна 1310 10 С, ниже 1250 С это соединение разлагается на ортованадат и оксид кальция, поэтому на диаграммах фазовых соотношений тетраванадат кальция не показан. [57]
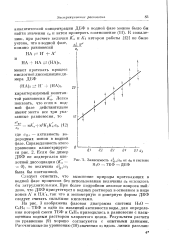 |
Зависимость a Azs от as в системе Н 0 - ТБФ - ДБФ. [58] |
На рис. 3 изображена фазовая диаграмма системы ШО - СеНб - ТБФ и одна из изолиний активности воды, для определения которой смеси ТБФ и СеНе приводились в равновесие с насыщенным водным раствором хлористого цезия. Результаты расчета по уравнению ( 9) хорошо согласуются с опытными данными. [59]
На рис. 141 представлена фазовая диаграмма системы этан-вода. Подобная общая характеристика может быть применена ко всем углеводородным системам. Точка Е является квадрупольной: в ней существует две жидкие фазы ( вода и углеводород), одна твердая фаза ( гидрат) и газовая фаза. [60]
Страницы: 1 2 3 4