Полная фазовая диаграмма
Cтраница 2
Большинство названных выше работ было выполнено для бинарных смесей состава 50 / 50 или для разбавленных растворов того же состава. Полные фазовые диаграммы, позволяющие оценивать степень смешения для каждого конкретного случая, получить гораздо сложнее в основном из-за того, что равновесие устанавливается в течение очень длительного времени. [16]
 |
Фазовая диаграмма церия. [17] |
Температура плавления этой фазы должна возрастать с повышением давления. Полная фазовая диаграмма европия должна быть похожа на диаграммы рубидия и стронция. [18]
Хотя фазовая диаграмма для бинарной системы трехмерна ( см. рис. 35.1), границей между двумя фазами в равновесной системе является поверхность. Сечение полной фазовой диаграммы, например сечение плоскостью температура - состав на рис. 35.1, пересекает эту поверхность по кривой. Выбор на этом пересечении температуры или состава полностью определяет равновесие. [19]
Хотя фазовая диаграмма для бинарной системы трехмерна ( см. рис. 35.1), границей между двумя фазами в равновесной системе является поверхность. Сечение полной фазовой диаграммы, например сечение плоскостью температура - состав на рис. 35.1, пересекает эту поверхность по кривой. Выбор на этом пересечении температуры или состава полностью определяет равновесие. [20]
 |
Расчет энтальпии плавления по. [21] |
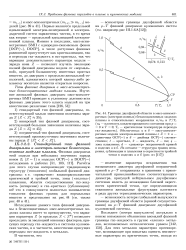
Это подтверждается и рис. 11, представляющим собой полную фазовую диаграмму коллагена, разумеется, в чистой воде. Любая точка на этой диаграмме, расположенная под асимметричной колоколообразной кривой, соответствует упорядоченному кристаллическому состоянию коллагена, а выше этой кривой - неупорядоченному, аморфному. Конечно, кривая не может быть продолжена вправо слишком далеко: при высоких нагрузках произойдет уже не плавление, а разрыв волоконец. Но тем не менее видно, что в ограниченном диапазоне температур и нагрузок напряжение может повышать Гпл; подобная обратная связь присуща только полимерам и обусловлена их конфигурационным полиморфизмом. [22]
Рассматриваемый тип перехода уникален в том смысле, что не требует одновременного участия многих молекул. Поэтому он развивается на очень малом ограниченном участке полной фазовой диаграммы, где не проявляются межмолекулярные взаимодействия. При увеличении концентрации спиральных макромолекул эти взаимодействия уже начинают проявляться, усиливая кооперативный характер перехода. С увеличением концентрации полимера переход из одномерного постепенно превращается в трехмерный. Таким образом, в концентрированных системах переход спираль - клубок даже с формальной точки зрения становится неотличимым от обычного плавления плотно упакованной кристаллической фазы. [23]
Система NH3 - N2 была изучена при температурах от 90 до 175 С и давлениях до 16000 бар. На рис. 1 - 8 и 1 - 9 приведены полная фазовая диаграмма и критическая кривая. [24]
Первые являются предельной идеализацией электрон-позитронной и электрон-дырочной систем заряженных частиц, в то время как вторые - предельной идеализацией электрон-ионной плазмы. Именно в последних, масс-асимметричных БМП с однородно-сжимаемым фоном ( ОСР (), DOCP, в числе доступных фазовых равновесий присутствует как кристаллизация, так и переходы газ-жид кость и газ-кристалл, так что вариация дополнительного параметра модели - заряда иона Z - позволяет изучать эволюцию полной фазовой диаграммы модели от нормальной, присущей большинству известных простых веществ, до диаграмм с предельно аномальной топологией, адекватность которой какому-либо реальному носителю является открытым вопросом. [26]
Для нитратов лития и калия получены кривые растворимости в зависимости от концентрации перекиси водорода с четкими разрывностями. Измерения электропроводности показывают, что эти соли диссоциируют в перекиси водорода так же, как и в воде, но электропроводность кислот в перекиси водорода ниже, чем в воде, что, вероятно, нужно объяснить меньшей подвижностью водородного иона в перекиси водорода. Измерения электропроводности использованы и для обнаружения реакции кислот или солей с перекисью водорода с образованием перекисных соединений. Доказано существование ряда аддитивных соединений с перекисью водорода. Некоторые ссылки, приведенные в табл. 58, относятся к этим пероксигидратам; дальнейшее обсуждение этого вопроса и ссылки па эту и другую литературу приведены в гл. Лишь очень небольшое число таких систем изучено достаточно подробно для представления полных фазовых диаграмм. [27]
Страницы: 1 2