Термодинамический баланс
Cтраница 1
Термодинамический баланс на катоде целесообразно сравнить с точным балансом. [1]
Термодинамические балансы устанавливают связь между потоками по каждому из веществ, энергии и энтропии, которыми система обменивается с окружением, а также возникновением этих величин в системе и скоростью изменения их количества. Все потоки далее мы будем суммировать, считая входящие потоки положительными, а выходящие - отрицательными. В отличие от конвективного потока диффузионный зависит от различия между интенсивными переменными исследуемой системы в точке, куда он входит или откуда выходит и интенсивными переменными окружения. Кроме того, будем использовать следующие обозначения: j - индекс потока, ej Vj, - внутренняя энергия и обьем одного моля соответствующего потока, a PJ - его давление, hj ej PJVJ - мольная энтальпия, hdj - энтальпия в потоке, поступающем диффузионно, qj - j - й поток тепла, Na - мощность, производимая системой. [2]
Термодинамические балансы связывают интенсивность и составы потоков, поступающих в систему, скорости химических превращений в ней и производство энтропии. Они же позволяют найти производство энтропии в неоднородной изолированной системе, когда подсистемы обмениваются друг с другом веществом и энергией. [3]
Термодинамический баланс системы очистки вода - амины значительно, лучше, чем при очистке только аминами. [4]
Во всех этих случаях термодинамические балансы, подобные (4.62), показывают, что суммарные затраты энергии на потенциалостатирование пропорциональны производству энтропии. [5]
Покажем, как из термодинамических балансов вытекают выражения для производства энтропии. [6]
Переменные, входящие в условия термодинамических балансов, как и значение сгть, в свою очередь могут зависеть от внешних факторов и от параметров самой системы ( поверхности контакта, характер гидродинамики потоков и пр. Таким образом, эти уравнения выделяют в плоскости параметров некоторую область, которую будем называть областью реализуемых значений параметров или областью реализуемости. [7]
При анализе возможности образования газовой плазмы рассматривается термодинамический баланс энергии в диэлектрике. Внутренняя часть потока носителей заряда может быть рассмотрена как бы находящейся внутри внешней области, выполняющей роль оболочки, препятствующей обмену энергией между внутренней областью и веществом диэлектрика вне ее. Такая адиабатическая модель позволяет считать, что кинетическая энергия носителей заряда затрачивается только на изменение внутренней энергии диэлектрика в этой области. При этом для каждого диэлектрика имеет место такое минимальное значение необходимого изменения внутренней энергии единицы объема диэлектрика Ас, при котором возникает начальный участок канала неполного пробоя. Таким образом, величина Ас может рассматриваться как энергетический критерий пробоя диэлектрика. [8]
Как было видно для всех рассмотренных примеров, из уравнений термодинамических балансов следует, что показатель эффективности использования энергии в термодинамических системах ( технический КПД) монотонно уменьшался с ростом производства энтропии т, т.е. с ростом необратимых потерь энергии. Величина а зависит от кинетики тепло - и массообменных процессов, а также кинетики химических реакций. Уравнения кинетики связывают диссипативные потоки энергии и вещества с интенсивными переменными взаимодействующих подсистем. [9]
В этой главе приведены математические модели систем и записаны уравнения термодинамических балансов, изложена общая схема исследования термодинамических систем в классе процессов заданной интенсивности, даны выражения для производства энтропии в типовых процессах и для обратимых оценок их эффективности. [10]
Стационарный тепловой режим характеризуется неизменностью температурного поля во времени вследствие наступления термодинамического баланса между источниками и поглотителями тепловой энергии. Нестационарный тепловой режим характеризуется зависимостью температурного поля от времени. [11]
В силу условий цикличности интегралы за период [ 0, г ] от правых частей в уравнениях термодинамических балансов (1.45) - (1.47) равны нулю. Если режим системы статический, то переменные состояния неизменны и левые части уравнений термодинамических балансов равны нулю. [12]
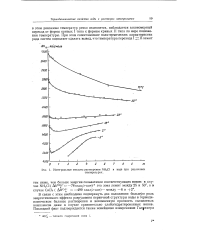 |
Интегральные теплоты растворения NHjCl в воде при различных. [13] |
В связи с этим необходимо подчеркнуть два положения: большую роль энергетического эффекта разрушения первичной структуры воды в термодинамическом балансе растворения и несомненную прочность сольватных комплексов даже в случае сравнительно слабогидратированных ионов. [14]
В том случае, когда разделение осуществляется за счет циркуляции рабочего тела с поочередным поглощением им примеси в первом полуцикле ( абсорбция или адсорбция) и выделением во втором полуцикле ( десорбция), выражение для термического КПД, близкое к (1.79), но включающее химические потенциалы потоков, можно получить из термодинамических балансов для рабочего тела. [15]
Страницы: 1 2