Атмосферный аммиак
Cтраница 1
 |
Отношение NH3 / NH4 в аэрозолях. [1] |
Атмосферный аммиак был уже давно обнаружен в дождевой воде. Как и в случае SO2 и МО2, лишь недавно было установлено, что он существует главным образом в газовой фазе. В табл. 23 приведены некоторые данные. [2]
Одним из источников атмосферного аммиака является почва. Находящиеся в почве органические вещества подвержены микробиологической деструкции. Аммиак является одним из продуктов разрушения органических веществ. [3]
Это позволяет избежать возможного загрязнения подкисленной пробы абсорбцией атмосферного аммиака. [4]
Это позволяет избежать возможное загрязнение подкисленной пробы абсорбцией атмосферного аммиака. [5]
Этот способ консервирования позволяет избежать возможного загрязнения подкисленной пробы абсорбцией атмосферного аммиака. [6]
Мы видим, что данные по дождевой воде дают ценную информацию относительно происхождения атмосферного аммиака, и выводы, полученные из этих данных, находятся в хорошем согласии с непосредственными измерениями NH3 в воздухе, которые рассматривались в разд. [7]
Для анализа низких концентраций аммония следует усовершенствовать обе системы, пропуская используемый воздух через разбавленную соляную кислоту, чтобы очистить его от содержания атмосферного аммиака. Ошибки, вызванные содержанием атмосферного аммиака, можно также уменьшить, накрывая сосуды с пробами алюминиевой фольгой, которую можно прорвать, когда потребуется вылить пробу. [8]
Следует отметить подцикл круговорота аммиака и окислов азота через атмосферу, особенно если учесть, что этот подцикл регулирует масштабы развития биосферы. Источниками атмосферного аммиака служат биохимические процессы в почве и, в первую очередь, аммонификация. Окисляясь, аммиак дает основную массу окислов азота в атмосфере. Получающаяся в процессе денит-рификации закись азота ответственна за содержание окислов азота в стратосфере, которые каталитически разрушают озон, защищающий живое вещество биосферы от губительного действия жесткого ультрафиолетового излучения. [9]
Для анализа низких концентраций аммония следует усовершенствовать обе системы, пропуская используемый воздух через разбавленную соляную кислоту, чтобы очистить его от содержания атмосферного аммиака. Ошибки, вызванные содержанием атмосферного аммиака, можно также уменьшить, накрывая сосуды с пробами алюминиевой фольгой, которую можно прорвать, когда потребуется вылить пробу. [10]
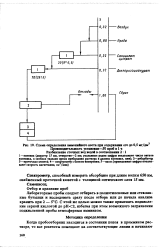 |
Схема определения аммонийного азота при содержании его до 0 5 мг / дм3. [11] |
Лабораторные пробы следует отбирать в полиэтиленовые или стеклянные бутылки и исследовать сразу после отбора или до начала анализа хранить при 2 - 5 С. С этой же целью можно также применять подкнсле-ние серной кислотой до рН2, избегая при этом возможного загрязнения подкисленной пробы атмосферным аммиаком. [12]
Лабораторные пробы следует собирать в полиэтиленовые или стеклянные бутыли. Их следует анализировать как можно быстрее или же до начала анализа хранить при 2 - 5 С. Можно также применять подкисление серной кислотой до рН2, что обеспечивает предотвращение возможного загрязнения подкисленной пробы атмосферным аммиаком. [13]
Лабораторные пробы следует собирать в полиэтиленовые или стеклянные бутыли. Их следует анализировать как можно быстрее или же до начала анализа хранить при 2 - 5 С. Можно также применять подкис-ление серной кислотой до рН 2, что обеспечивает предотвращение возможного загрязнения подкисленной пробы атмосферным аммиаком. [14]
 |
Объем пробы в зависимости от концентраций азота. [15] |
Страницы: 1 2