Метод - кондуктометрическое титрование
Cтраница 2
Метод кондуктометрического титрования растворов фенолятов ( Сиповский и др., 1961) с учетом поправки на явление гидролиза с достаточной точностью позволяет определить количество едкого натра, связываемого фенолами. [16]
Методом кондуктометрического титрования определяют многие катионы и анионы. Нитратом серебра титруют хлорид, бромид, иодид, цианид, тиоцианат, оксалат, ванадат, тартрат, сали-цилат и некоторые другие анионы. Титрованием в среде 90 % - но-го спирта определяют С1 - в природных водах при содержании порядка 10 мкг. Содержание 1 - и С1 - в смеси может быть определено без предварительного разделения. Титрование ацетатом или хлоридом бария применяют для определения сульфата, хромата, карбоната, оксалата, цитрата и других анионов обычно при добавлении в анализируемый раствор спирта. Сульфаты таким методом определяют в природных водах и аналогичных объектах. [17]
Методом кондуктометрического титрования были определены [1259] концентрации кислоты, связанной с поверхностью латексов сополимера итаконовой кислоты со стиролом, и свободной кислоты в водной фазе. [18]
Однако метод кондуктометрического титрования позволяет проводить определение аминофенолов, основываясь на реакции их нейтрализации сильными основаниями или сильными кислотами. [19]
Предложен метод кондуктометрического титрования ионов меди цитратом лития [349], ионы цинка не мешают определению. Ионы алюминия и железа ( III), мешающие определению, маскируют фторидом аммония. Метод применен для анализа латуней и бронз. [20]
Преимущество метода кондуктометрического титрования заключается также в том, что в некоторых случаях представляется возможным использовать реакции, при которых вещества реагируют не в стехиометрических отношениях. При этом стандартизацию рабочего раствора проводят кондуктометрическим методом при тех же условиях по титрованным растворам определяемых веществ. [21]
В основу метода кондуктометрического титрования могут быть положены различные химические реакции. [22]
К достоинствам метода кондуктометрического титрования относится возможность высокоточных измерений даже в очень разбавленных растворах. В отличие оттитриметрии с визуальными индикаторами кондукто-метрическое титрование пригодно для анализа окрашенных или мутных растворов. Графический способ нахождения конечной точки титрования позволяет избежать трудностей, возникающих из-за замедления реакции вблизи конца титрования и снижающих точность фиксирования конечной точки. [23]
В основу методов кондуктометрического титрования могут быть положены различные химические реакции. [24]
К преимуществам метода кондуктометрического титрования относится возможность дифференцированного определения веществ в многокомпонентных смесях в водных растворах. Другим преимуществом метода является возможность определений в окрашенных и мутных растворах, а также в присутствии окислителей или восстановителей, ограничивающих, например, применение кислотно-основных индикаторов. [25]
Рассмотрим применение метода кондуктометрического титрования для исследований коагуляции на примере золя AsgSs. [26]
Имеется классификация методов кондуктометрического титрования, которая основана на типах реакций, используемых для определения содержания того или иного соединения. В этих методах используются следующие реакции: 1) кислотно-основного взаимодействия; 2) комплексообразования; 3) осаждения; 4) окисления - восстановления. [27]
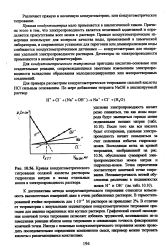 |
Кривая кондуктометрического титрования соляной кислоты раствором гидроксида натрия и вклад отдельных ионов в электропроводность раствора. [28] |
К достоинствам метода кондуктометрического титрования относится возможность высокоточных измерений даже в очень разбавленных растворах. В отличие от титриметрии с визуальными индикаторами кондуктометрическое титрование пригодно для анализа окрашенных или мутных растворов. Графический способ нахождения конечной точки титрования позволяет избежать трудностей, возникающих из-за замедления реакции вблизи конца титрования и снижающих точность фиксирования конечной точки. [29]
 |
Мост для измерения электропроводности. [30] |
Страницы: 1 2 3 4