Метод - комплексонометрическое титрование
Cтраница 2
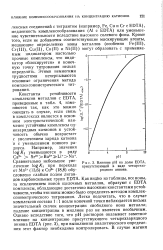 |
Влияние рН на долю EDTA, присутствующей в виде четырехзарядного аниона. [16] |
Этими немногими трудностями исчерпываются основные ограничения метода комплексонометрического титрования. [17]
Для определения фтора в золе углей может быть применен метод комплексонометрического титрования. [18]
Следует указать, что гафний реагирует с комплексо-яом III в тех же условиях, что и цирконий, поэтому метод комплексонометрического титрования дает возможность определять либо один из этих элементов в отсутствии другого, либо их суммарное количество. [19]
Аминополикарбоновые кислоты типа ЭДТА образуют довольно прочные комплексы почти со всеми - многовалентными катионами, что и положено в основу метода комплексонометрического титрования. Эта общая способность к комплексообразованию является, с одной стороны, преимуществом, так как с помощью одного-един-ственного титрованного раствора можно определять большое число различных элементов, а с другой стороны - недостатком, так как она обусловливает низкую избирательность определений. [20]
В дополнение к стандартным гравиметрическим и колориметрическим методам Мейтес [292] дает перечисление пригодных химических методов анализа, к которым он отнес способы осаждения силикат-иона в виде соли кобальта с последующим определением методом комплексонометрического титрования и в виде соли азотистого основания, которая затем титруется хлорной кислотой. [21]
В некоторых случаях вместо описанных выше методов пользуются методом титрования заместителя. Метод комплексонометрического титрования заместителя основан на том, что Mg - HOHbi дают с комплексоном менее устойчивое комплексное соединение ( р / С 8 7), чем подавляющее большинство других катионов. [22]
При этом используют химически чистый препарат РЬ ( МОз) 2 - Концентрацию приготовленного раствора проверяют одним из описанных в литературе методов. Для этой цели может быть использован метод комплексонометрического титрования в аммиачной среде с применением эриохрома черного Т в качестве индикатора. [23]
В силу различных причин были Получены отрицательные результаты при использовании следующих индикаторов ( рН 0 5 - 1 5): пирокатехинового, фиолетового, 2 4-дисульфобензаурин - 3 3-дикарбоиовой кислоты; нитрозо - Н - соли: эриохром черного Т; 1 8-диокси - 2 - ( 2 -карбоксибензолазо) - нафталин-3 6-дисульфокис-лоты; кислотного хром темно-синего; 2 4-диоксибензол - 1-азо - 1 - 2-оксинафталин - 4-сульфокислоты и дифениламин-2 - сульфо-кислота-4 - азо-2 - диоксинафталин-3 6-дисульфокислоты. Последние два индикатора просто разрушались азотной кислотой. Метод комплексонометрического титрования Pu ( IV) с арсеназо I был применен П. Н. Палеем и Н. Е. Кочетковой ( 1959 г.) для определения содержания плутония в его двуокиси. Растворение двуокиси проводили подобно описанному выше в методе окислительно-восстановительного титрования Pu ( III) ванадатом аммония ( стр. [24]
Константы устойчивости комплексов металлов с EDTA, приведенные в табл. 4, изме-няются так, как это можно ожидать в случае, если связь в комплексах является в основ-ном электростатической: наименее устойчивы комплексы однозарядных катионов и устойчивость обычно возрастает с увеличением заряда катиона и с уменьшением ионного радиуса. Сравнительно небольшое увеличение log / Ci при переходе от Мп2 ( 13 6) к Си2 ( 18 8) обусловлено слабым полем лиган-дов карбоксильных групп EDTA. Как видно из таблицы, все ионыг за исключением ионов щелочных металлов, образуют с EDTA комплексы, обладающие достаточно высокими константами устойчивости, чтобы эти ионы можно было определять методом комплексонометрического титрования. Легко подсчитать, что в случае комплексов состава 1: 1 возле конечной точки наблюдается весьма значительный скачок концентрации свободного иона металла; падение концентрации в миллион раз не является необычным. Однако вследствие того, что рН растворов оказывает заметное влияние на концентрацию присутствующего четырехзарядного аниона EDTA ( рис. 3), при выполнении аналитического определения этот фактор необходимо контролировать. [25]
Индикаторами точки эквивалентности обычно служат лиганды, образующие с анализируемым ионом окрашенное комплексное соединение. Например, индикатор хромоген черный ( см. табл. 16.1) с кальцием и магнием образует комплексы [ Са Ind ] - и [ Mg Ind ] - красного цвета. В результате титрования раствора винно-красного цвета, содержащего ионы кальция, магния и индикатор, раствором комплексона Ш кальций связывается в более прочный комплекс с комплексоном, в точке эквивалентности анионы индикатора освобождаются и придают раствору синюю окраску. Этот метод комплексонометрического титрования используется, например, для определения общей жесткости воды. [26]
Страницы: 1 2