Метод - уайт
Cтраница 1
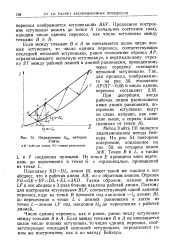 |
Определение Nor методом Уайта. [1] |
Метод Уайта [3] является видоизменением метода Бей-кера. [2]
 |
Определение NQT методом Симпсона. АВ - рабочая линия. ОС-линия равновесия. [3] |
Метод Уайта несколько сложнее метода Бейкера, однако при методе Уайта не требуется построения средней линии; кроме того, построение ступенек можно начинать с любого конца рабочей линии. [4]
Метод Уайта ( частично заимствовано из статьи D. [5]
Метод Уайта основан на известном положении о том, что к случаях, показанных на рис. 1, когда примесь и основной компонент образуют простую эвтектику, при кристаллизации из раствора выделяется в кристаллическом состоянии только один основной компонент, а примеси остаются в жидкой фазе. Для такого типа растворов Уайт использует количественную связь понижения температуры кристаллизации с количеством имеющихся в веществе примесей. [6]
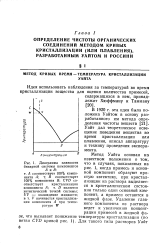 |
Диаграмма плавкости бинарной системы компонентов. [7] |
Метод Уайта основан на известном положении о том, что в случаях, показанных на рис. 1, когда примесь и основной компонент образуют простую эвтектику, при кристаллизации из раствора выделяется в кристаллическом состоянии только один основной компонент, а примеси остаются в жидкой фазе. [8]
Впоследствии принципы метода Уайта были распространены на вещества, кристаллизующиеся в области отрицательных температур. [9]
Необходимо отметить, что в основе всех методов расчета коэффициентов активности, кроме методов Уайта, Ли и Коула и Джу и Коула, лежит условие постоянства температуры. Поэтому найденные по этим методам коэффициенты активности, строго говоря, применимы лишь для расчета изотермических данных о равновесии. При определении по этим коэффициентам активности изобарных данных о равновесии, требующихся для расчетов процессов ректификации, не учитывается изменение коэффициентов активности с температурой. [10]
Необходимо отметить, что в основе всех методов расчета коэффициентов активности, кроме методов Уайта, Ли и Коула и Джу и Коула, лежит условие постоянства температуры. Поэтому ( найденные по этим методам коэффициенты активности, строго говоря, применимы лишь для расчета изотермических данных о равновесии. При определении по этим коэффициентам активности изобарных данных о равновесии, требующихся для расчетов процессов ректификации, не учитывается изменение коэффициентов активности с температурой. [11]
Страницы: 1