Метод - электронный удар
Cтраница 3
Потенциал появления молекулярных ионов, определенный методом электронного удара, совпадает с адиабатическим в том случае, если равновесные межъядерные расстояния в молекуле и молекулярном ионе равны. [31]
Франклин, Дайблер и Риз [1598] методом электронного удара измерили потенциал появления N ( 16 0 0 1 эв) в реакции HNs N NH. Используя значения 71 66 ккал / моль для теплоты образования HNs [1848] и 15 576 эв для потенциала ионизации Na ( см. выше), была вычислена энергия диссоциации Do ( NH) 82 7 ккал / моль, хорошо согласующаяся со значением, полученным линейной экстраполяцией. [32]
Для увеличения точности определения потенциалов ионизации методом электронного удара применяют специальные методы, увеличивающие моно-энергетичность электронов. Использование такого стандарта более надежно, если ионизационные потенциалы объекта и стандарта имеют близкие значения. [33]
В классических опытах Франка и Герца методом электронного удара были определены не только потенциалы возбуждения, но и ионизационные потенциалы ряда атомов. [34]
 |
Зависимость первых потенциалов ионизации атомов от порядкового номера элемента. [35] |
Одним из способов определения энергии ионизации является метод электронного удара. Он заключается в том, что атомы в газе облучаются электронами, получившими энергию под действием разности потенциалов. Минимальное значение разности потенциалов, которое обеспечивает энергию свободному электрону, достаточную для выбивания электрона из атома, называют потенциалом ионизации. [36]
Одним из способов определения энергии ионизации является метод электронного удара. Он заключается в том, что атомы в газе облучаются электронами, получившими энергию под действием разности потенциалов. [37]
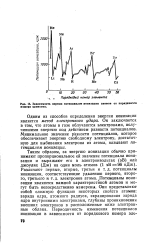 |
Зависимость первых потенциалов ионизации атомов от порядкового номера элемента. [38] |
Одним из способов определения энергии ионизации является метод электронного удара. Он заключается в том, что атомы в газе облучаются электронами, получившими энергию под действием разности потенциалов. Минимальное значение разности потенциалов, которое обеспечивает энергию свободному электрону, достаточную для выбивания электрона из атома, называют потенциалом ионизации. [39]
 |
Теплота образования ионов карбония. [40] |
Теплоты образования ионов карбония вычислены на основании метода электронных ударов. [41]
Значения Я, могут быть измерены, методом электронного удара. Этим же методом можно также оценить энергию диссоциации соединений, в частности углеводородов, по С-С - скязи. Энергии диссоциации могут быть также определены термохимическим методом. [42]
Ионизационный потенциал трифторметильного радикала, определенный непосредственно методом электронного удара, значительно выше ( 10 1 эв) 18 19, и Котрелл20 полагает, что, комбинируя это значение со значением потенциала появления иона трифторметильного радикала СРз из двух фторированных этапов, он точнее оценивает энергию разрыва связи С-1-С: 97 ккал / моль для гексафторэтана и 90 ккал / моль для 1 1 1-трифторэтана. Однако Прайс5 считает, что значение потенциала ионизации трифторметильного радикала, найденное методом электронного удара, в действительности само по себе выше примерно на 0 5 эв, так что в процессе диссоциации осколки приобретают еще большую кинетическую энергию. Если же рассчитать энергию разрыва связи в гексафторэтане, исходя из теплоты образования трифторметильного радикала и собственно этана, получают значение 69 ккал / моль20, что подтверждается некоторыми кинетическими соображениями. [43]
Ионизационный потенциал трифторметильного радикала, определенный непосредственно методом электронного удара, значительно выше ( 10 1 эв) 18 19, и Котрелл20 полагает, что, комбинируя это значение со значением потенциала появления иона трифторметильного радикала СРз из двух фторированных этанов, он точнее оценивает энергию разрыва связи С-С: 97 ккал / моль для гексафторэтана и 90 ккал / моль для 1 1 1-трифторэтана. Однако Прайс5 считает, что значение потенциала ионизации трифторметильного радикала, найденное методом электронного удара, в действительности само по себе выше примерно на 0 5 эв, так что в процессе диссоциации осколки приобретают еще большую кинетическую энергию. Если же рассчитать энергию разрыва связи в гексафторэтане, исходя из теплоты образования трифторметильного радикала и собственно этана, получают значение 69 ккал / моль20, что подтверждается некоторыми кинетическими соображениями. [44]
В принципе, для определения ЕА пригоден также метод электронного удара. При столкновении электрона с молекулой может происходить диссоциация молекулы с образованием отрицательного осколочного иона. Измерения потенциала появления этого иона и начальной кинетической энергии осколков позволяют определить сродство к электрону осколка. [45]
Страницы: 1 2 3 4