Потенциометрический метод
Cтраница 3
Потенциометрический метод применим к Сплавам, содержащим 0 5 % Cd вовсе не содержащим цинка и серебра. [31]
 |
Принципиальная схема измерений по методу амперметра - вольтметра. [32] |
Потенциометрический метод обеспечивает высокую точность при. В этом случае падение напряжения на образце сравнивается с падением напряжения на последовательно включенном эталонном сопротивлении. Падение напряжений ED и EN измеряется потенциометром ( см. гл. [33]
Потенциометрический метод и метод импульсной поляризации основаны на измерении электродного лотенциала поверхности металла под покрытием в зависимости от плотности тока. [34]
Потенциометрический метод может быть использован для измерения активной концентрации различных ионов в растворах электролитов. При этом каждый раз необходимо подбирать материал индикаторного электрода, для которого определяемый ион был бы потенциал-определяющим. В дальнейших разделах, при описании методов измерения некоторых ионов, разбираются свойства соответствующих индикаторных электродов. [35]
Потенциометрический метод наиболее широко применяют для определения активности ионов водорода, характеризующей кислотные или щелочные свойства раствора. [36]
Потенциометрический метод определенна концентрации водородных ионов. [37]
Потенциометрический метод позволяет провести ряд определений за короткий промежуток времени ( несколько минут) и в большинстве случаев без предварительного разделения компонентов. Необходимо также отметить, что в природных объектах ( в частности, в почвах) для различных процессов обычно решающую роль играет не концентрация ионов ( или молекул), а их активность, которая отражает реальное участие ионов в почвообразовании и питании растений. [38]
Потенциометрический метод применяют тогда, когда в гальваническом элементе возможно обратимое протекание окислительно-восстановительной реакции с участием исследуемой системы Ох - Red. Естественно, существуют варианты потенциометрического метода, обусловленные особенностями изучаемых систем. Для многих гетерогенных окислительно-восстановительных систем, образованных металлом и его ионом, стандартный окислительный потенциал определяют с помощью гальванического элемента без жидкостного соединения. [39]
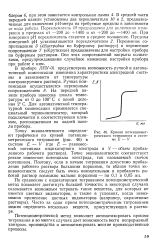 |
Кривая потенциомет-рического титрования в системе Е - V. [40] |
Потенциометрический метод позволяет автоматизировать процесс титрования и во многих случаях дает возможность вести непрерывный контроль производства и автоматизировать многие производственные процессы. [41]
 |
График чувствительности кислородомера во времени при установке в аэротенке. [42] |
Потенциометрический метод основан на применении в качестве индикаторного электрода из металлического таллия. Вспомогательным служит стандартный электрод. Достоинством этого метода является то, что для его реализации не требуется специальная аппаратура. Для этой цели пригодны преобразователи и арматура датчиков рН - метров. Таллие-вьш электрод в течение длительной непрерывной работы в воде не требует очистки своей поверхности. Очевидно, этому способствует индифферентность к окислительно-восстановительным реакциям с другими веществами. [43]
Потенциометрический метод применяется также и при титровании по другим методам объемного анализа. [44]
Потенциометрический метод основан на измерении изменений электрохимического потенциала электрода, погруженного в раствор одноименных ионов, во время титрования. Величина потенциала, устанавливающегося между электродом и раствором, зависит от концентрации соответствующих ионов и поэтому может служить для количественного их определения. Электрод, по потенциалу которого судят о концентрации определяемых ионов, называется индикаторным. Величину его потенциала сравнивают с постоянной величиной потенциала второго электрода - электрода сравнения, в качестве которого выбирают нормальный водородный или каломельный электрод. При титровании концентрация определяемого иона уменьшается и в эквивалентной точке резко изменяется потенциал, что служит показателем конца титрования. Потен-циометрическое титрование может быть применено во всех описанных выше методах объемного анализа. [45]
Страницы: 1 2 3 4