Электровесовой метод
Cтраница 1
Электровесовой метод является одним из наиболее точных методов определения меди. [1]
Электровесовой метод основан на выделении из раствора определяемого элемента ( или вещества) с помощью, электролиза. При этом взвешивают электрод до анализа, погружают его в исследуемый раствор, пропускают постоянный ток, по окончании электролиза снова взвешивают электрод с выделившимся веществом и производят вычисление. Электрический ток здесь как бы играет роль реактива, осаждающего на одном кз электродов нужный компонент из раствора. [2]
Электровесовой метод / 3 / является наиболее распространенный при определении больших количеств меди. Этот ыетод дает наиболее точные результаты при условии, что удалены все мешающие электролизу элементы ( металлы, стоящие в ряду напряжений ниже меди) и если проведено извлечение последних следов меди из электролита. [3]
Электровесовой метод основан на выделении из раствора определяемого элемента ( или вещества) с помощью электролиза. При этом взвешивают электрод до анализа, погружают его в исследуемый раствор, пропускают постоянный ток, по окончании электролиза снова взвешивают электрод с выделившимся веществом и производят вычисление. Электрический ток здесь как бы играет роль реактива, осаждающего на одном из электродов нужный компонент из раствора. [4]
Электровесовой метод является одним из наиболее точных методов определения меди. [5]
Электровесовым методом чаще всего анализируют растворы, содержащие медь, никель, кобальт, свинец. [6]
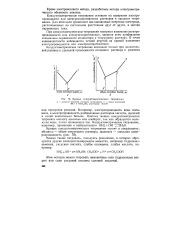 |
Кривые кондуктометрического титрования. [7] |
Кроме электровесового метода, разработаны методы электрометрического объемного анализа. [8]
При электровесовом методе определяемое вещество ( Си, РЬ02, AgCl) выделяют из раствора при помощи электролиза. [9]
При электровесовом методе определяемое вещество ( Си, РЬ02, AgCl) выделяют из раствора при помощи электролиза. Электрод взвешивают до анализа, погружают в исследуемый раствор, пропускают постоянный ток, снова взвешивают с выделившимся веществом и делают вычисление. [10]
Существует два варианта электровесового метода. По второму варианту постоянный ток возникает при погружении в анализируемый раствор так называемой гальванической пары и в этом случае внешнего источника тока не требуется. Этот вариант электровесового анализа называют методом внутреннего электролиза. [11]
В отличие от электровесового метода кулонометрически можно определять также те вещества, которые не осаждаются на электроде, а остаются в растворе или удаляются в окружающую атмосферу. [12]
Существуют два варианта электровесового метода. По второму варианту постоянный ток возникает при погружении в анализируемый раствор так называемой гальванической пары, и в этом случае внешнего источника тока не требуется Этот вариант электровесового анализа называют методом внутреннего электролиза. [13]
Существуют два варианта электровесового метода. По второму варианту постоянный ток возникает при погружений в анализируемый раствор так называемой гальванической пары, и в этом случае внешнего источника тока не требуется. Этот вариант электровесового анализа называют методом внутреннего электролиза. [14]
Существуют два варианта электровесового метода. По второму варианту постоянный ток возникает при погружений в. Этот вариант электровесового анализа называют методом внутреннего электролиза. [15]
Страницы: 1 2