Потенциодинамический метод
Cтраница 1
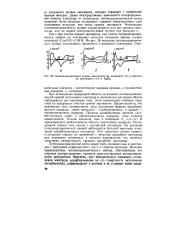 |
Потенциодинамические кривые платинового ( а, иридиевого ( б и родиевого ( в электродов в 4 6 н. HaS04. [1] |
Потенциодинамический метод может быть применен как к электродам с развитыми поверхностями, так и к гладким металлам. Большим преимуществом потенциодинамического метода, обусловившим его широкое распространение, является довольно высокая воспроизводимость результатов. [2]
Потенциодинамический метод может быть применен как к электродам с развитыми поверхностями, так и к гладким металлам. Большим преимуществом потенциодинамического метода, обусловившим его широкое распространение, является довольно высокая воспроизводимость результатов. Вероятно, при периодическом изменении потенциала электрода адсорбированные на его поверхности загрязнения де-сорбируются, диффундируют в раствор и не успевают затем адсорбироваться. [3]
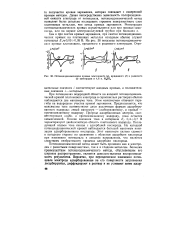 |
Потенциодинамические кривые платинового ( а, иридиевого ( б и родиевого ( в электродов в 4 6 н. HaS04. [4] |
Потенциодинамический метод может быть применен как к электродам с развитыми поверхностями, так и к гладким металлам. Большим преимуществом потенциодинамического метода, обусловившим его широкое распространение, является довольно высокая воспроизводимость результатов. [5]
Потенциодинамический метод может быть использован вместо метода кривых заряжения при выполнении любой из работ, которые представлены на с. При достаточно высоких скоростях развертки потенциала ( 20 мВ / с) при выполнении этих работ вместо платинированного платинового электрода можно использовать гладкий платиновый. [6]
Потенциодинамический метод имеет определенное преимущество в информативности перед методом кривых заряжения, как и любой метод определения производной искомой функции перед интегральным методом. Фактически рассмотренную выше адсорбцию водорода и кислорода на платине можно трактовать как процесс образования адатомов, так как слой Яадс возникает из ионов Н3О значительно раньше ( на 0 35 - 0 4 В), чем начинается выделение молекулярного водорода, а адсорбированные атомы кислорода образуются за счет разряда молекул воды или ионов ОН - при потенциалах, лежащих отрицательнее обратимого кислородного на 0 5 - 0 6 В. Образование адатомных слоев ( или субмонослоев) до достижения равновесных потенциалов соответствующих систем описано в настоящее время при адсорбции большого числа катионов ( Си2, Ag, Pba, Bi3, Sn2, Hgjj, T1 и др.) и анионов ( I -, S2 - и др.) на электродах из Pt, Rh, Pd, Аи и других материалов. Причина этого явления состоит в том, что энергия связи между металлом-субстратом и атомом-адсорбатом оказывается во многих случаях значительно больше, чем энергия связи между атомами в фазе адсорбата. [7]
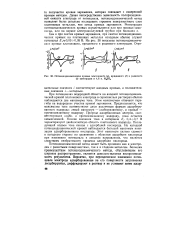 |
Потенциодинамические кривые платинового ( а, иридиевого ( б и родиевого ( в электродов в 4 6 н. HaS04. [8] |
Потенциодинамический метод может быть применен как к электродам с развитыми поверхностями, так и к гладким металлам. Большим преимуществом потенциодинамического метода, обусловившим его широкое распространение, является довольно высокая воспроизводимость результатов. [9]
Потенциодинамический метод также называют хроновольтам-перометрией с линейной разверткой потенциала, что точно отражает функциональную зависимость потенциала от времени. Хро-новольтамперометрия с линейной разверткой потенциала на ртутном капельном электроде называется классическим полярографическим методом, а на твердых микроэлектродах - полярографией на твердых электродах. Аналогично для гальванодинамического метода применяется название хроногальванометрия с линейной разверткой тока. [10]
Потенциодинамическим методом показано, что некоторые СЖК обладают степенями защиты более 95 % в сероводородсодержащих минерализованных средах, имитирующих пластовые воды нефтяных месторождений Республики Башкортостан. [11]
Выполненные потенциодинамическим методом исследования показали, что гетероциклические азотсодержащие соединения, в качестве модели которого был взят хинолин, хемосорбционно взаимодействуют с поверхностью железа, приводя ее в пассивное состояние. В еще большей степени такой эффект проявляется при воздействии на поверхность железа эпоксидно-каменноугольной композиции. При этом защитный эффект изменяется симбатно степени заполнения поверхности железного электрода хемосорбированными компонентами антикоррозионной композиции. [12]
В потенциодинамическом методе при помощи потенциостата осуществляется быстрое изменение ( развертка) потенциала электрода со скоростью от 6 до 100 мВ / с. При изменении потенциала электрода в определенной области потенциалов происходит ионизация адсорбированного водорода, и скорость этого процесса фиксируется по изменению силы тока, возникающего в системе. В результате могут быть получены / - ф-кривые, отражающие изменение состояния адсорбированного на поверхности водорода. Наличие двух характерных максимумов на 1-ф-кривых позволяет разграничивать формы адсорбции. [13]
Проведены замеры скорости коррозии соединений потенциодинамическим методом. Плотность тока коррозии определяли экстраполяцией тафелевых участков поляризационных кривых, снятых в неингибированной и ингибированной средах, до значений, соответствующих потенциалам коррозии. [14]
По-видимому, при работе с помощью потенциодинамического метода создаются условия, аналогичные тем, которые имеют место для анодных переходных максимумов. [15]
Страницы: 1 2 3