Метода - расчет - равновесие
Cтраница 1
Методы расчета равновесий жидкость - пар все в большей степени базируются на физически обоснованных моделях жидкой фазы, на новых вариантах уравнений состояния. [1]
Методы расчета равновесия между жидкостью и паром представляют большой практический интерес, так как: позволяют уменьшить объем экспериментальных исследований и исключают необходимость аналитического определения состава фаз. [3]
Методы расчета равновесия на основе стандартных или формальных ОВ потенциалов, в том числе расчет констант устойчивости комплексов в произведения растворимости, проиллюстрированы большим числом важных для аналитической химии примеров. [4]
Методы расчета равновесий, описанные в § 160 и 161, основанные на использовании уравнений, выражающих температурную зависимость Ср, на практике отнюдь не всегда бывают такими простыми, как в приведенных примерах. Основной причиной их усложнений является наличие точек фазовых переходов ( плавления, кипения, полиморфных превращений) того или другого из компонентов реакционной системы в рассматриваемом температурном интервале. Каждая кривая индивидуальной теплоемкости претерпевает излом в такой точке. Каждое уравнение АСР / ( Г) применимо лишь в пределах интервала между двумя такими точками одного или разных веществ. [5]
Методы расчета равновесия между жидкостью и паром представляют большой практический интерес, так как позволяют уменьшить объем экспериментальных исследований и исключают необходимость аналитического определения состава фаз. [7]
Во всех случаях методы расчета равновесия в сложных системах основываются на использовании данных для входящих в их состав более простых систем. [8]
Известно, что все методы расчета равновесия в реальных многокомпонентных системах являются эмпирическими, основаны на различных допущениях о свойствах многокомпонентной системы и сводятся к определению ряда констант, не имеющих ясного физического смысла, по данным для составляющих бинарных систем. При этом предполагают, что свойства составляющих бинарных систем одинаково хорошо описываются уравнением для многокомпонентных систем. Однако встречающиеся на практике системы относятся к разным классам растворов и далеко не всегда могут быть описаны одним и тем же уравнением. [9]
Чтобы приближенный и точный методы расчетов равновесия автора стали подлинно универсальными, необходимо обеспечить возможность проведения расчетов реакций, в которых участвуют пары металлов, не в две ступени ( с поправкой на агрегатное превращение), а в одну. Для этого нужно, чтобы вспомогательная таблица функций М, N и Ас содержала данные не только для твердых и жидких металлов, но и паров их. [10]
Принятый в настоящее время метод расчета равновесий с помощью третьего закона термодинамики основывается на определении абсолютных энтропии всех участвующих в реакции веществ. [11]
Вместе с тем разработанные автором методы расчета равновесия в том виде, в каком они - были предложены первоначально, значительно осложнялись, когда необходимо было учитывать полиморфные или агрегатные превращения реагентов. [12]
В связи с изложенным лучше всего разработаны методы расчета равновесия жидкость - пар для систем с идеальной паровой фазой. [13]
 |
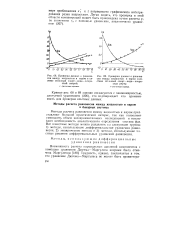
Равновесный состав конденси - JQ рованной фазы при 1900 К в зависимое - п IH от давления ТКП и СН4. [14] |
Основной недостаток и основные ошибки рассмотренного выше метода расчета равновесия вызваны не тем, что в ЭВМ вводятся термодинамические сведения не всех участвующих в равновесии веществ, а игнорированием образования растворов этих веществ в конденсированной фазе и особенно игнорированием широкой области гомогенности карбида титана. [15]
Страницы: 1 2 3