Диазотат-ион
Cтраница 1
Диазотат-ион проявляет свойственную амбидентным анионам двойственную реакционную способность не только при протонировании, но и в реакциях алкилирования. [1]
Диазотат-ион, подобно енолят-иону ( гл. [2]
Диазоанион ( диазотат-ион) является общим ионом для диазо-гидрата и нитрозамина. Существует в двух формах: син - и анти-диазотатной. [3]
Диазоанион ( диазотат-ион), отрицательный заряд в котором распределен между кислородом и азотом, связанным с ароматическим остатком, является общим ионом для диазогидрата и нитро-зоамина. Первичный ароматический нитрозоамин, также недиссоциированная форма диазосоединения, находится в таутомерном равновесии с диазогидратом. [4]
Такое различие в поведении от - и анти-форм диазотат-ионов обусловлено тем, что сын-диазотат обладает более высокой основностью по сравнению с янты-диазотатом и протонируется поэтому по атому кислорода. Менее основный з / даш-диазотат протонируется по азоту с образов aHHeMN - нитрозоамина. Различие в основности двух форм диаэотатов хорошо объясняет смещение равновесия в сторону менее основного и, следовательно, более стабильного анти-диазотата при нагревании. Обратная изомеризация в некоторых случаях наблюдается только при облучении Уф-спектром. [5]
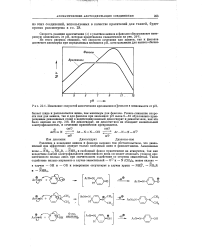 |
Изменение скоростей азосочетания ариламинов и фенолов в зависимости от рН. [6] |
Резкое снижение скорости как для аминов, так и для фенолов при значениях рН выше 9 - 10 обусловлено превращением диазониевых солей в недиссоциированный диазогидрат и диазотат-ион, как это было описано на стр. Ни диазогидрат, ни диазотат-ион не обладают значительной электрофильностью, и сочетание практически прекращается. [7]
Возникновение различных форм диазосоединений зависит от концентрации ионов водорода в растворе: в кислом растворе равновесие сдвигается в сторону образования солей диазония; наоборот, при повышении рН среды оно сдвигается вправо, в сторону образования диазотат-иона. [8]
Возникновение различных форм диазосоединений зависит от концентрации ионов водорода в растворе: в кислом растворе равновесие сдвигается в сторону образования солей диазония; наоборот, при пдвышении рН среды, оно сдвигается вправо, в сторону образования диазотат-иона. [9]
Таким образом, возникновение различных форм диазосоединений зависит от концентрации ионов водорода в растворе: в кислом растворе равновесие сдвигается в сторону образования солей диазония; наоборот, при повышении рН среды оно сдвигается вправо, в сторону образования диазотат-иона. [10]
Таким образом, возникновение различных форм диазосоединений зависит от концентрации ионов водорода в растворе; в кислом растворе равновесие сдвигается в сторону образования солей диазония; наоборот, при повышении рН среды оно сдвигается вправо, в сторону образования диазотат-иона. [11]
Резкое снижение скорости как для аминов, так и для фенолов при значениях рН выше 9 - 10 обусловлено превращением диазониевых солей в недиссоциированный диазогидрат и диазотат-ион, как это было описано на стр. Ни диазогидрат, ни диазотат-ион не обладают значительной электрофильностью, и сочетание практически прекращается. [12]
Этот вывод подтверждается тем, что анизол ( метиловый эфир фенола) с большинством солей диазония не реагирует, хотя в других реакциях электрофильного ароматического замещения фенол и анизол одинаково высоко реакциоиноспособны. При увеличении рН раствора выше десяти скорость замедляется потому, что ион диазония переходит в неактивный диазотат-ион. [13]
 |
Изменение скоростей азосочетания ариламинов и фенолов в зависимости от рН. [14] |
Из этого рисунка очевидно, что скорости сочетания как аминов, так и фенолов достигают максимума при определенных значениях рН, хотя максимум для аминов обычно бывает шире и располагается ниже, чем максимум для фенолов. Резкое снижение скорости как для аминов, так и для фенолов при значениях рН выше 9 - 10 обусловлено превращением диазониевых солей в недиссоциированный ди-азогидрат и диазотат-ион, как это было описано в разд. Ни диазогидрат, ни диазотат-ион не обладают значительной электрофильностью, и сочетание практически прекращается. [15]
Страницы: 1 2