Миграция - ион - водород
Cтраница 1
Миграции ионов водорода из анодной камеры в катодную препятствует селективная проницаемость аниони-товой мембраны. Если раствор соляной кислоты достаточно концентрирован, на аноде выделяется хлор, который может быть собран. В данном случае электрохимический процесс имеет те же преимущества: экономия на химических реагентах, отсутствие загрязнения амина солью и получение ценных побочных продуктов. [1]
Плотность тока при наводороживании определяет интенсивность миграции ионов водорода к катоду. С увеличением DK эта интенсивность растет и достигает максимального значения при плотностях тока в пределах 1 - 10 а / дм2 в зависимости от условий эксперимента. Дальнейшее увеличение DK не приводит к усилению эффекта наводо-роживания в связи с ограниченной возможностью поверхности металла поглощать водород, а также в связи с образованием вокруг катода сплошной зоны пузырьков водорода, препятствующих контакту электролита с металлом. [2]
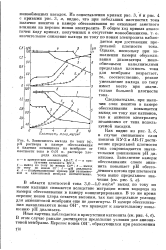 |
Зависимость выхода по току ( т, рН раствора в камере обессоливания и падения потенциала на мембране от плотности тока в 0 01 н. растворе хлорида кальция. [3] |
В области плотностей тока 3 0 - 4 0 ма / смг выход по току по ионам кальция снижается вследствие миграции ионов водорода из камеры обессоливания в камеру концентрирования. В то же время перенос ионов хлора остается высоким, так как предельные условия для анионитовой мембраны еще не достигнуты. В камере обессоливания накапливаются ионы ОН, что приводит к значительному повышению рН диализата. [4]
Изменение энергии активации ионной проводимости в растворах КС1 при варьировании давления аналогично изменению энергии активации вязкого течения. Однако в растворах НС1 изменения энергии активации этих двух процессов при варьировании давления заметно различаются, поскольку, как полагают, при относительно низком давлении скорость миграции ионов водорода определяется вращением молекул воды вдоль траектории мигрирующего иона, но при давлении выше 1400 бар вращение затруднено и скорость определяющим фактором становится перескок протона от одной молекулы воды к другой. Удовлетворительного объяснения этому экспериментальному факту не найдено. [5]
Аномально высокая электропроводность растворов кислот и оснований, наблюдающаяся не только в водных растворах, но и в других растворителях, молекулы которых содержат ОН-группу, связана с ионами водорода и гидроксила, так как именно эти ионы отличают кислоты и основания от других электролитов. Таким образом, аномально высокая подвижность ионов водорода, низкая энергия активации их миграции, неправдоподобно малые ионные радиусы - все это приводит к заключению, что механизм миграции ионов водорода, а также ионов гидроксила, обнаруживающих подобные же аномалии, должен быть иным, чем для всех остальных ионов. [6]
Скорости переноса протона между ионом водорода и молекулами растворителя были непосредственно измерены с помощью ЯМР в воде ( 54) и метаноле ( 35) и косвенно - с помощью данных по подвижности водородного иона в различных других растворителях. Чтобы использовать данные по подвижности протона, нужно предположить, что экспериментальная величина подвижности водородного иона ( цн) является суммой двух величин, одна из которых представляет собой подвижность, обусловленную переносом протона, а другая - нормальную подвижность, обусловленную миграцией сольвати-рованного иона водорода как кинетической частицы. Нормальную подвижность можно считать приблизительно равной подвижности иона натрия ( ш), для которого член, обусловленный переносом протона, очевидно, равен нулю. [7]
В работе [2] показано, что восстановление протекает только в случае непосредственного соприкосновения частички WO3 с поверхностью электрода. В допущении существования атомов водорода нет никакой необходимости, так как трехокись вольфрама является полупроводником п-типа. К тому же следует добавить, что начальное высокое сопротивление может уменьшиться за счет миграции ионов водорода, так как в окисле устанавливается электростатическое поле значительной напряженности. Юнг [289] допускает проникновение в окисел в местах дислокаций ионов Н, имеющих малые размеры. Шмидт [273] также указывает на возможность внедрения протона в окисел. По его мнению, протоны создают донорные центры, обусловливающие проводимость окисла. [8]
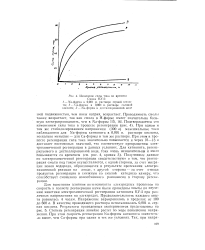 |
Изменение силы тока во времени. [9] |
При этом в процессе регенерации сила тока значительно повышается и через 10 - 13 ч достигает постоянных значений, что соответствует прекращению электрохимической регенерации в данных условиях. Полученные данные по электрохимической регенерации свидетельствуют о том, что регенерация смолы подтоком осуществляется, с одной стороны, за счет миграции ионов водорода, образующихся в результате протекания электрохимической реакции на аноде, с другой стороны - за счет отвода продуктов регенерации в смежную со смолой катодную камеру, что способствует смещению ионообменного равновесия в сторону регенерации. [10]
Считается, что энергия активации определяется в первую очередь работой создания полости в растворителе, куда ион переходит из предыдущего положения равновесия. Энергия активации, подсчитанная из температурной зависимости скорости движения ионов, оказалась примерно одинаковой для всех ионов, кроме ионов водорода. Ее значение для водных растворов колеблется между 16 и 18 кДж - моль-1, что довольно близко к энергии активации вязкого течения воды; обычно это связывают с тем, что перескоки совершают гидратированные ионы, хотя возможны и другие объяснения. Энергия активации миграции ионов водорода составляет всего лишь 11 кДж - моль-1. [11]
В то время как произведение величин подвижности и вязкости для иона натрия остается почти постоянным, за исключением несколько повышенного значения в воде, значения этого произведения для водородного иона аномально высоки в гидроксильных растворителях и в осо - бенности в воде. Последнее согласуется с тем фактом, что подвижность водородного иона в воде превосходит более чем в 5 раз-подвижность любого другого иона, кроме иона гидроксила. Нужно далее иметь в виду, что, хотя для большинства ионов значение энергии активации ионной подвижности составляет около 4 ккал в воде при 25 С, для водородного иона это значение равно только 2 8 ккал. Отсюда следует, что механизм миграции иона водорода в водном растворе отличен от механизма миграции других ионов. [12]
Наличие фазово-выраженного оксида или другого соединения не исключает адсорбционного механизма пассивности. Вместе с тем возникновение пленок существенно изменяет условия взаимодействия между металлом и электролитом, в том числе и адсорбционное взаимодействие. Пленка может образоваться также в результате пересыщения раствора в прианодной зоне плохо или хорошо растворимым соединением и его кристаллизации на аноде. Возможно также образование и кристаллизация гидроксида, оксида или основной соли на аноде в результате миграции ионов водорода из прианодного слоя. Так, на поверхности свинцового анода в серной кислоте во врем: я электролиза образуются кристаллические зародыши твердой фазы PbSO4, которые разрастаются в сплошной изолирующий слой. [13]
Страницы: 1