Екор
Cтраница 3
Величина Екор сильно различается для основного и возбужденных состояний системы, причем до сих пор отсутствуют надежные теоретические формулы ее вычисления. Недооценка - ЕКор, определяющей в значительной степени такую важную характеристику системы, как энергия связи, является существенным недостатком метода МО. Но еще более важным его недостатком следует признать невозможность надежного сравнения энергий системы в нейтральном и ионном состояниях, ибо в э ом случае корреляционная энергия еще менее сравнима, чем в ее основном и возбужденном состояниях. Наконец, даже наиболее точный из методов МО, основанных на концепции самосогласованного поля, метод ХФ не позволяет вычислить малые разности энергий мультиплетных уровней, знание которых необходимо при расшифровке спектроскопических данных. [31]
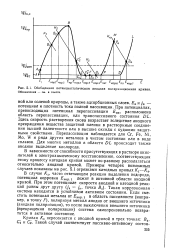 |
Обобщенная потенциостатическая анодная поляризационная кривая. Обозначения - ск. ш тексте. [32] |
Такая коррозионная система находится в устойчивом активном состоянии. Если сместить потенциал металла от Екор. F), поляризуя металл анодно от внешнего источника ( анодная поляризация), то после выключения внешнего источника ( прекращения поляризации) система самопроизвольно возвратится в активное состояние. [33]
Для этого в уравнения (4.19) следует вместо Е подставить Екор из (4.36), а га заменить на гкор. [34]
Для этого в уравнения (4.19) следует вместо Е подставить Екор из (4.36), а га заменить на гкор. [35]
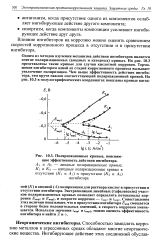 |
Поляризационные кривые, поясняющие эффективность действия ингибитора. [36] |
Сопоставление этих величин показывает, что в присутствии ингибитора - Екор смещается в сторону более положительных значений, а скорость коррозии уменьшается. [37]
Скорость растворения цинка является скоростью его электрохимической коррозии; она может быть охарактеризована в единицах плотности тока и называется плотностью тока коррозии. Плотность тока коррозии, а следовательно, и скорость коррозии, определяемая ординатой от Екор до пересечения с поляризационной кривой, может быть найдена не только по количеству цинка, перешедшего в раствор в единицу времени, но и по количеству выделившегося водорода, так как при коррозионном потенциале скорости этих процессов равны. [38]
Первоначально измеряют потенциал коррозии в отсутствие тока Екор. Потом электрод катодно поляризуют в течение 30 секунд при потенциале на 200 мВ отрицательнее Екор. После этого снимают анодную поляризационную кривую при скорости развертки потенциала 10 мВ / с. Фиксируют величины токов с помощью миллиамперметра или высокоомного вольтметра. [39]
Потенциал питтингообразования ( - ЕПо) характеризует нарушение пассивного состояния. Он является наименьшим потенциалом, при достижении которого начинается стабильный рост образования пит-тингов. Епо - Екор служит характеристикой склонности металла к питтинговой коррозии и влияния внешних параметров. Этот показатель и определяют при постановке исследований по данной методике. [40]
С исследовали коррозионный питтинг, образовавшийся не при Екор ( в отсутствие внешней поляризации), а при потенциалах, задаваемых потенциостатом ( Т 5 ч), но это значение Е соответствует примерно значению Екор. [41]
Изменение рН раствора при постоянной величине Сак практически не влияет на величину Ерп. При определенной критической величине рН происходит изменение электрохимического состояния металла - реализуется возможность его самопассивации. В последнем случае ( в средах от слабокислых до слабощелочных) Екор сталей также слабо зависит от рН раствора, то есть их базисы А-Брп и Д ЕПк, а, следовательно, и питтингостоикость, практически не зависит от рН среды. [42]
Изменение рН раствора при постоянной величине Сак практически не влияет на величину Ерп. При определенной критической величине рН происходит изменение электрохимического состояния металла - реализуется возможность его самопассивации. В последнем случае ( в средах от слабокислых до слабощелочных) Екор сталей также слабо зависит от рН раствора, то есть их базисы А рп и А пк, а, следовательно, и питтингостоикость, практически не зависит от рН среды. [43]
Изменение рН раствора при постоянной величине Сак практически не влияет на величину Ерп. При определенной критической величине рН происходит изменение электрохимического состояния металла - реализуется возможность его самопассивации. В последнем случае ( в средах от слабокислых до слабощелочных) Екор сталей также слабо зависит от рН раствора, то есть их базисы Д - Ерп и & Епк, а, следовательно, и питтингостойкость, практически не зависит от рН среды. [44]
Практическое значение П.м. исключительно велико. Она обеспечивает необходимую коррозионную стойкость конструкций и изделий, изготовляемых из разл. Широко применяется самопассивация металлич. Такого же результата добиваются введением в среду дополнит, окислителя или повышением его концентрации. Во всех этих случаях должны выполняться условия: Екор Еарп или Екор Етг. [45]
Страницы: 1 2 3 4