Микрокалориметрия
Cтраница 1
Микрокалориметрия также применялась, например, для контроля за протеканием кислородно-водородных реакций титрования на дисперсных платиновых катализаторах [179], но микрокалориметрия по сути своей является методом научного исследования и малопригодна как рутинный метод определения удельной поверхности. [1]
Сканирующая микрокалориметрия выявляет в ряде случаев последовательность пиков теплоемкости при плавлении глобулы. Ясно видны три пика теплоемкости. Это может свидетельствовать о раздельном плавлении доменов в глобуле или об отщеплении ионов Н, происходящем при разных температурах в разных участках. В сочетании с рентгенографией и другими методами микрокалориметрия дает полезную информацию. [3]
Методом микрокалориметрии определены энтальпии растворения алкоксидов бора, mpem - бутилата лития и mpem - бутилтриоктилбората лития в гептане и хлороформе. Рассчитаны энтальпии сольватации алкоксидов бора в этих растворителях. Энтальпии сольватации алкилборатов пропорциональны их молекулярным рефракциям, а хлороформ не является инертным растворителем для mpem - бутилата лития. [4]
Методом микрокалориметрии установлено значительное влияние перемешивания на теилоту процесса, что указывает на определенную роль диффузии в заряженной оболочке противоиона. [5]
Методом микрокалориметрии определены энтальпии растворения алкоксидов бора, mpem - бутилата лития и mpem - бутилтриоктилбората лития в гептане и хлороформе. Рассчитаны энтальпии сольватации алкоксидов бора в этих растворителях. Энтальпии сольватации алкилборатов пропорциональны их молекулярным рефракциям, а хлороформ не является инертным растворителем для mpem - бутилата лития. [6]
 |
Преобразователь для измерения электрических величин.| Простейший микрокалориметр. [7] |
Объектами изучения в микрокалориметрии являются различные биохимические и физико-химические процессы. [8]
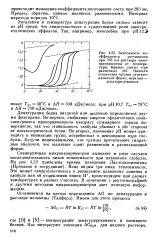
Адсорбция присадок оценивалась методами микрокалориметрии и контактной разности потенциалов, потенциальная склонность граничных слоев к развитию химической реакции определялась по адгезионной прочности пленок, которая, в свою очередь, оценивалась по уменьшению Величины Д К. Чем меньше изменение ( уменьшение) величины А КРП, тем прочнее адсорбционные слои, образованные присадками на металле. [9]
Фундаментальным методом исследования процессов структурной релаксации является метод дифференциальной сканирующей микрокалориметрии. [10]
Анализ дифференциальных функций, в частности дифференциальных тепловых эффектов, полученных с помощью микрокалориметрии, показывает, что вхождение первых органических противоионов в сорбент резко отличается от связывания последующих ионов. Наибольшую роль в этом отличии играет не столько неравноценность фиксированных ионов в ионите, сколько кооперативный эффект взаимодействия. Как видно из рис. 4, в случае кооперативной изотермы сорбции гемоглобина на катионите КМДМ-2, отличающейся положительным значением второй производной по концентрации, проявляется переход от экзотермического к эндотермическому взаимодействию, а следовательно, и к положительной энтропии сорбции. Здесь полифункциональность проявляется уже в дополнительном взаимодействии между сорбированными ионами. Аналогичная картина наблюдается и при кооперативной сорбции антибиотика олеандо-мицина на поликонденсационном карбоксильном катионите КРФФУ. [11]
Микрокалориметрия также применялась, например, для контроля за протеканием кислородно-водородных реакций титрования на дисперсных платиновых катализаторах [179], но микрокалориметрия по сути своей является методом научного исследования и малопригодна как рутинный метод определения удельной поверхности. [12]
Рассчитайте и сравните результаты определения теплоты реакции изомеризации / гяюкозы в D-фруктозу при Т - 321.15 К, полученные методами хроматографии и микрокалориметрии. [13]
В заключение отметим, что для изучения тепловых эффектов процессов денатурации белков и нуклеиновых кислот и взаимодействия этих биополимеров с ионами металлов и гид-роксония в последнее время широко и успешно применяется микрокалориметрия. Тепловые эффекты этих процессов довольно малы. ДНК составляет около 4 0 ккал на моль мономерных единиц. Однако с помощью специальных приборов - дифференциальных сканирующих микрокалориметров, впервые сконструированных у нас в стране под руководством П. Л. Привалова, измерения становятся возможными. [14]
В заключение отметим, что для изучения тепловых эффектов процессов денатурации белков и нуклеиновых кислот и взаимодействия этих биополимеров с ионами металлов и гидроксония в последнее время широко и успешно применяется микрокалориметрия. Тепловые эффекты этих процессов довольно малы. ДНК составляет около 4 0 ккал на моль мономерных единиц. [15]
Страницы: 1 2