Микроколичество - определяемый элемент
Cтраница 1
Микроколичества определяемых элементов соосаждаются с сульфидом кадмия, который получается из раствора хлорида кадмия при добавлении к нему раствора сульфида натрия. Сначала добавляют меньшую часть раствора CdCl2 и весь раствор Na2S, необходимые для образования коллоидного раствора сульфида кадмия. [1]
Микроколичества определяемых элементов соосаждаются с сульфидом кадмия, который получается из раствора хлорида кадмия при добавлении к нему раствора сульфида натрия. Сначала добавляют половину нужного количества раствора хлорида кадмия и весь раствор сульфида натрия. Образуется коллоидный раствор сульфида кадмия в растворе сульфида натрия. [2]
Микроколичества определяемых элементов соосаждаются с сульфидом кадмия, который получается из раствора хлорида кадмия при добавлении к нему раствора сульфида натрия. Сначала добавляют меньшую часть раствора CdCl2 и весь раствор NaaS, необходимые для образования коллоидного раствора сульфида кадмия. [3]
Микроколичества определяемых элементов соосаждаются с сульфидом кадмия, который получается из раствора хлорида кадмия при добавлении к нему раствора сульфида натрия. Сначала добавляют половину нужного количества раствора хлорида кадмия и весь раствор сульфида натрия. Образуется коллоидный раствор сульфида кадмия в растворе сульфида натрия. [4]
Для очистки веществ и для выделения микроколичеств определяемых элементов широко применяют методы экстрагирования органическими растворителями. Если для определения примеси применяется экстракционно-флуориметрический метод, то буферный раствор и остальные реактивы также можно очистить экстракцией. Например, такой прием был использован А. Ф. Фиолетовой при определении оксихинолином алюминия в солях магния ( стр. [5]
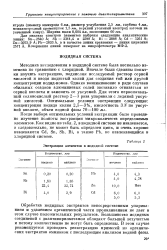 |
Экстракция элементов в иодидной системе. [6] |
После выбора оптимальных условий экстракции было проведено изучение полноты экстракции микроколичеств определяемых элементов. Как видно из табл. 2, в иодидной системе не извлекается, а следовательно, не может быть определен цинк, и очень хорошо извлекаются Cd, Sn, Sb, Bi, а также РЬ, не извлекающийся в хлоридной системе. [7]
Кинетические методы основаны на измерении скорости так называемой индикаторной реакции, катализируемой микроколичествами определяемого элемента. К проведению эксперимента в аналитических целях предъявляются те же требования, что и в в обычных кинетических исследованиях. Главенствующую роль играет, естественно, постоянство температуры, которую поддерживают в пределах 0 2 С. Строго должны быть регламентированы концентрации реагентов, в том числе и кислоты, если ее протоны расходуются в окислительно-восстановительном процессе. Концентрация индифферентных солей не должна варьировать в широких пределах. Дополнительные поправки необходимы в случае одновременного протекания каталитической и некаталитической реакции. [8]
Эталоны готовили путем внесения микроколичеств определяемого элемента в виде раствора соли известной концентра-ции в такой же кварцевый бюкс, как и для образца, и после высушивания в сушильном шкафу помещали в алюминиевый контейнер и ставили на облучение. [9]
Резюмируя вышеизложенное, можно предположить, что наиболее широкое практическое значение может найти лишь тот метод определения малых содержаний бериллия, в котором рационально сочетаются высокая чувствительность используемых реагентов с оптимальным методом разделения компонентов. Свидетельством этого является растущее число работ, посвященных методам, предусматривающим именно предварительное отделение бериллия. Особенно перспективны в этом отношении приемы, позволяющие одновременно отделять и концентрировать микроколичества определяемого элемента. Таков метод колоночной распределительной хроматографии, благодаря которому для определения микроколичеств бериллия становится возможным использование любого высокочувствительного органического красителя. [10]
Страницы: 1