Минерал - портландцемент
Cтраница 1
Минералы портландцемента имеют преимущественно ионную кристаллическую структуру, в связи с чем рассмотрим механизм растворения кристалла, в узлах ячеек которого находятся поочередно расположенные ионы соответствующих химических элементов. В кристаллах такого типа разноименно заряженные ионы связаны друг с другом силами электростатического притяжения, и работа, необходимая для нарушения этих связей, измеряется энергией кристаллической решетки. [1]
Минералы портландцемента и многих других минеральных ( неорганических) вяжущих веществ представляют собой оксиды или чаще соли щелочных и щелочноземельных металлов ( Na, К, Са Mg) и очень слабых кремниевых, алюминиевых и железистых кислот. [2]
При диссоциации минералов портландцемента энергии решетки противостоит энергия гидратации, зависящая от сил, действующих между полярными молекулами воды и ионами минералов твердой фазы. При соприкосновении воды с поверхностью минерала, ионы, составляющие его кристаллическую решетку, притягиваются противоположно заряженными частицами молекул воды. [3]
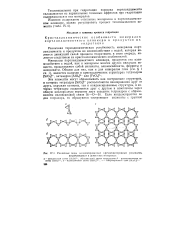 |
Различные виды конденсированных кремнекислородных радикалов. [4] |
Различная термодинамическая устойчивость минералов портландцемента и продуктов их взаимодействия с водой, которая является движущей силой процесса гидратации, в свою очередь, является следствием их кристаллохимических особенностей. [5]
Различная термодинамическая устойчивость минералов портландцемента и продуктов их взаимодействия с водой - движущая сила процесса гидратации, являющаяся следствием кри-сталлохимических особенностей их микроструктур. Минералы портландцементного клинкера, продуктов его взаимодействия с водой, как и минералы многих других вяжущих веществ, представляют собой силикаты, алюминаты, ферриты и алюмосиликаты. Существуют как островные структуры, в которых тетраэдры [ SiO располагаются изолированно друг от друга, окружая катионы, так и конденсированные структуры, в которых тетраэдры соединяются друг с другом в комплексы через общую кислородную вершину двух соседних тетраэдров с образованием силоксановой связи Si-О - Si. [6]
По коллоидно-химической гипотезе Михаэлиса минералы портландцемента гидратируются в твердом состоянии, не переходя в раствор, путем присоединения воды по поверхности. Зерна портландцемента покрываются при этом оболочкой гелеобразных продуктов гидратации, объем которых примерно в 2 раза больше объема исходной негидратированной частицы. В результате этого зерна сращиваются между собой, а их срастание постепенно упрочняется в ходе коллоидно-химических процессов упрочнения гелей. [7]
Для протекания нормальной реакции гидратации минералов портландцемента, обусловливающих твердение камня, необходима вода. Недостаток воды замедляет процессы гидратации и изменяет структуру цементного камня. В скважине расход воды на гидратацию в некоторой степени компенсируется поступлением в цементный камень пластовых вод и фильтрата из глинистой корки. [8]
Основу асбестоцемента составляют продукты гидратации минералов портландцемента ( гидросиликаты, гидроалюминаты кальция и др.) и волокна хризотил-асбеста. [9]
Повышение температуры значительно ускоряет реакции гидратации минералов портландцемента, а следовательно, и твердения цементного камня. Для камня из портландцемента наибольшая прочность соответствует интервалу температур 80 - 100 С. Дальнейшее повышение температур снижает механическую прочность камня, поэтому для цементирования скважин с забойными температурами, превышающими 100 С не рекомендуется применять чистый портландцемент. [10]
 |
Образцы цементного камня, разрушенные в среде газообразного сероводорода. [11] |
Коррозия выщелачивания происходит вследствие способности продуктов гидратации минералов портландцемента к гидролизу. Они представляют собой водные силикаты, алюминаты и ферриты кальция, а также гидроксид кальция. Большинство соединений в цементном камне устойчиво при рН11 и в присутствии определенной концентрации ионов кальция. При отсутствии химической агрессии необходимое значение рН и концентрация ионов кальция обеспечиваются наличием в порах цементного камня и у его поверхности ( если он находится в воде) насыщенного раствора гидроксида кальция, образующегося в результате выделения гидроксида кальция при гидролизе клинкерных минералов. Однако обновления пресной или мягкой воды у поверхности цементного камня достаточно для медленного его разрушения в результате постепенного вымывания Са ( ОН) 2 и последующего разрушения других соединений. [12]
Вторую группу образуют добавки, способные к обменным химическим реакциям с продуктами гидратации минералов портландцемента, из числа которых чаще других г, такие реакции вступает гидроксид кальция. Один из видов реакций, приводящих к образованию труднорастворимых гидроксидов, описан выше. Другой часто используемый вид обменных реакций приводит к образованию труднорастворимых сох ей кальция. К таким добавкам относятся борная кислота, виннокаменная ( или винная) кислота, щавелевая кислота, а также растворимые соли этих кислот. Труднорастворимые кальциевые соли этих кислот откладываются в виде плотной пленки вокруг частиц клинкера, препятствуя процессу гидратации. К этой группе добавок относятся самые сильные замедлители схватывания портландцементных суспензий. [13]
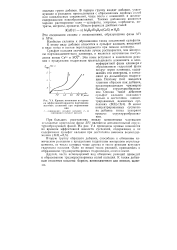 |
Кривые изменения во времс - трированных Цементных сус. [14] |
Вторую группу образуют добавки, способные к обменным химическим реакциям с продуктами гидратации минералов портландцемента, из числа которых чаще других в такие реакции вступает гидроксид кальция. Один из видов таких реакций, приводящих к образованию труднорастворимых гидроксидов, описан выше. [15]
Страницы: 1 2