Михельса
Cтраница 2
Хейман и Пирс [1940] вычислили значения В фторметана, измерив сжимаемость при низких давлениях порядка 0 5 атм в интервале 293 - 353 К. На основании экспериментальных р - V - Г - данных Михельс и Виссер [2891] определили значения второго вириального коэффициента в интервале 273 - 423 К и вычислили силовые постоянные межмолекулярного потенциала Стокмейера. [16]
На основании экспериментальных р - V - Г - данных Михельс и Недербрегт [2889] определили силовые постоянные межмолекулярного потенциала Леннарда-Джонса: к / k 148 2 К и 670 16 см3 / моль. Шамп, Мейсон, Ричардсон и Олтман [3606] из значений второго вириального коэффициента рассчитали силовые постоянные, которые хорошо согласуются с данными Михельса и Недербрегта. Эти значения силовых постоянных более надежны, чем значения e / k 148 К и fco 67 06 см3 / моль, полученные Корнером [1180] на основании кристаллографических данных. Спенсер и Фланнаган [3820] на основании экспериментальных данных предложили эмпирическое уравнение для теплоемкости метана. Следеский [3765] на основании литературных данных и с использованием уравнения состояния Бенедикта составил графики теплоемкости метана для интервала 297 - 1019 К и для давлений от 34 до 680 атм. [17]
По иронии судьбы, в социал-демократической партии власть находилась в руках небольшой клики людей, точно так же, как и в консервативных партиях, против которых она боролась. Согласно Михельсу, эти тенденции проявляются в любой крупномасштабной организации. [18]
Теоретические работы, помещенные в этой части, дают преимущественно описание электронной структуры соединений благородных газов. В некоторых из статей делается упор на низшие электронные состояния молекул с целью выяснения роли электронной структуры в формировании геометрии молекул или, в специальных случаях, в определении ядерной конфигурации. Статьи Аллена, Михельса, Джиллеспи и Лора с Липскомбом, по-видимому, попадают в эту категорию. Аллен наиболее сильно подчеркивает необходимость примирения положения инертных газов в периодической таблице со способностью некоторых из них к образованию простых молекул. [19]
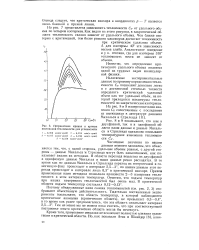 |
Пограничная кривая и кривые постоянной теплоемкости для углекислоты. [20] |
Численные значения по нашим данным немного занижены, что объясняется тем, что, с одной стороны, удельные объемы равные, с другой стороны - данные Михельса и Стриленда могут быть завышенными, как показывает анализ их методики. В области перехода вещества из двухфазной в однофазную данные Михельса и наши данные резко расходятся. В то время как по данным Михельса и Стриленда переход из гетерогенной в гомогенную фазу происходит в интервале 2 5 - 3, по нашим данным этот переход происходит в интервале лишь 0 3 в критической изохоре. Причем примененная нами методика позволила произвести 2 - 3 измерения теплоемкости в этом интервале температур. Отметим, что подъем температур при наших измерениях теплоемкостей был очень мал. [21]
По поводу несомненно реальных явлений анаэробного торможения Гаффрон отмечает, что длина инкубационного периода указывает скорее на медленное накопление продуктов брожения, чем на диссоциацию лабильного кислородного соединения. Зеленые расте ния лишены кислородного фермента, образующего спирты и органические кислоты ( см. главу VI); некоторые из этих продуктов могут быть ядовиты для фотосинтетического аппарата. Исследования Гафф-рона [10], Ноака, Пирсона и Михельса [13] и Михельса [16] показали, что анаэробное торможение сильно только в кислом растворе и менее выражено или даже совершенно отсутствует в щелочных буферных растворах. Отсюда Ноак с сотрудниками объясняют его образованием свободных кислот при брожении, например, молочной кислоты. [22]
По поводу несомненно реальных явлений анаэробного торможения Гаффрон отмечает, что длина инкубационного периода указывает скорее на медленное накопление продуктов брожения, чем на диссоциацию лабильного кислородного соединения. Зеленые расте ния лишены кислородного фермента, образующего спирты и органические кислоты ( см. главу VI); некоторые из этих продуктов могут быть ядовиты для фотосинтетического аппарата. Исследования Гафф-рона [10], Ноака, Пирсона и Михельса [13] и Михельса [16] показали, что анаэробное торможение сильно только в кислом растворе и менее выражено или даже совершенно отсутствует в щелочных буферных растворах. Отсюда Ноак с сотрудниками объясняют его образованием свободных кислот при брожении, например, молочной кислоты. [23]
Михельс [2887] экспериментально определил значения второго вириального коэффициента в интервале 273 - 423 К и подробно рассмотрел вопрос о применении уравнения Камерлинг-Оннеса к СОз в указанном температурном интервале. Он установил, что это уравнение лучше, чем другие уравнения состояния, передает р - V - Т - данные при давлениях выше 500 атм. Данные Мак-Кормака и Шнейдера хорошо согласуются с данными Михельса в пределах указанной точности эксперимента. Значения второго вириального коэффициента для температур 213 - 243 К, найденные Куком [1164], находятся в согласии сданными других исследователей. [24]
Первые точные измерения сжимаемости аргона проведены Оннесом и Кроммелином [3142] для низкотемпературного интервала 123 - 293 К и при давлениях от 1 до 62 атм. Позднее Крег [1209] получил более точные данные для указанного низкотемпературного интервала. Данные Холборна и сотрудников [2101, 2102, 2103, 2104] охватывают температурный интервал 73 - 673 К при давлениях до 105 атм. В работе Нури и сотрудников [3105] на основании измерений скорости ультразвука определена сжимаемость аргона от критической температуры до 523 К при давлениях до 1200 атм. Танкер и Мак-кон [3942] измерили сжимаемость аргона между 298 и448 К при давлениях от 30 до 125 атм. Бриджман [938, 939] определил р - V - Г - данные аргона при высоких давлениях до 15 000 атм в интервале 100 - 328 К. Наиболее точные р - V-ТЧданные получены Михель-сом и сотрудниками [2894] в интервале 273 - 423 К при давлениях до 2900 атм. В более поздней работе Михельс, Левелт и Де-Графф [2882] измерили сжимаемость аргона при температурах 118 - 248 К при давлениях до 1050 атм. [25]
Страницы: 1 2