Предэкс-поненциальный множитель
Cтраница 2
При сравнении скоростей молекулярного распада этана и распада его на два радикала СН3 следует учитывать не только энергии активации этих реакций, но и предэкс-поненциальные множители констант скоростей. [16]
Представление уравнения Аррениуса (1.3) в координатах линейной анаморфозы Ink f ( l / T) ( рис. 1.2) позволило рассчитать по методу наименьших квадратов численные значения энергии активации и предэкс-поненциального множителя для процесса окисления изопропилбензола на катализаторе АП-56 ( табл. 1.6 - 1.8), которые для свежего и отработанного катализаторов крупного и мелкого дробления достаточно близки - значения энергии активации лежат в пределах 52 - 60 кДж / моль. [17]
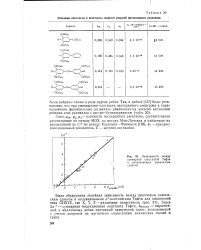 |
Спиновые плотности и константы скорости реакций феноксильных радикалов.| Зависимость между суммарной константой Тафта и исправленным химическим-сдвигом. [18] |
Здесь рм, pL, ps - плотности неспаренного электрона, соответственно рассчитанные по методу МОХ, по методу Мак-Лачлана и найденные из расщеплений на С13 по методу Карплуса-Френкеля [128]; &0 - предэкс-поненциальный множитель, Е - энергия активации. [19]
Вполне возможно, что пиролиз циклобутана - процесс, обратный простейшему [2 2] - циклоприсоединению, - не является синхронной реакцией. Считают 162 ], что предэкс-поненциальный множитель в уравнении Аррениуса указывает на ступенчатое разложение циклобутана, протекающее через образование тетраметиленового радикала. Кроме того, тот факт, что пиролиз цис - или / пранс-диметшщиклобутана ( 152) дает среди других продуктов смесь цис - и транс-бу-тенов [63], подтверждает бирадикальный механизм. Все же, если циклораспад - синхронная реакция, он должен относиться к типу I02S 02a ], и должен наблюдаться тот же стереохимический результат. [20]
Имеется довольно мало надежных сведений о бимолекулярных обменных реакциях в газах. Значения независимого от температуры члена А, соответствующие величинам предэкс-поненциального множителя, деленным на Т11 2, приводятся в третьем столбце. [21]
В сложных химических реакциях феноменологической мерой реакционной способности может быть эффективная константа скорости, а в элементарных реакциях - константа скорости элементарного акта. Константа скорости в соответствии с уравнением Аррениуса является функцией двух основных факторов: предэкс-поненциального множителя А и энергии активации. Энергия активации оказывает большее влияние на реакционную способность и, следовательно, играет первостепенную роль в определении реакционной способности. [22]
В сложных химических реакциях феноменологической мерой реакционной способности может быть эффективная константа скорости, а в элементарных реакциях - константа скорости элементарного акта. Константа скорости в соответствии с уравнением Аррениуса является функцией двух основных факторов: предэкс-поненциального множителя А и энергии активации. Энергия активации оказывает большее влияние на реакционную способность и, следовательно, играет первостепенную роль в определении реакционной способности. [23]
На самом деле соотношения этого типа не должны соблюдаться, так как в них не может быть постоянного предэкс-поненциального множителя. [24]
Иногда теорию активированного комплекса называют теорией абсолютных скоростей реакций. Но такое название неправильно, так как для расчета абсолютных скоростей химических реакций надо иметь возможность рассчитать не только предэкс-поненциальные множители, но и энергии активации. [25]
Во-первых, по Рогинскому, gk - E2, в то время как на рис. 115 видно, что в большом интервале значений с хорошей точностью выполняется lgk - E. Во-вторых, анализ зависимости k ( E), полученной в работе [56], показывает, что она не может объяснить увеличения предэкс-поненциального множителя ( по сравнению с нормальным) более чем на 6 - 8 порядков, в то время как экспериментально найденные значения отличаются от обычных на 10 - 20 порядков. [26]
Это означает, что активированный комплекс становится четырехэлектронным в отличие от обычного активированного комплекса, который в первом приближении можно рассматривать как трехэлектронный. Энергетически протекание такой реакции значительно облегчено, однако вероятность ее много меньше, чем вероятность реакции с трехэлектронным активированным комплексом. Последнее согласуется с экспериментально наблюдаемыми низкими значениями энергии активации и предэкс-поненциального множителя. [27]
В табл. 34 приведены данные о константах скоростей рекомбинации радикалов в углеводородных полимерах, поливинилхлориде и различных образцах тефлона. Сразу же обращают на себя внимание необычно большие значения предэкспоненциальных множителей в случае рекомбинации фторалкильных и алкильных радикалов. Как известно, для бимолекулярных реакций в газовой и жидкой фазе величина предэкс-поненциального множителя колеблется в пределах К) - 10 - 10 - 15 см3 / сек. [28]
 |
Зависимость доли непревращенной кислоты от критериального комплекса / г и Ft. [29] |
Расчет реактора по графику производят следующим образом. По требуемой степени превращения H2SO4 находят отношение Ск, L / Ск, о. Зная константу скорости реакции, рассчитанную по уравнению (2.84) с учетом среднего значения предэкс-поненциального множителя К 1 87 ( см. разд. [30]
Страницы: 1 2 3