Дифференциальная емкость - электрод
Cтраница 2
 |
Эквивалентные схемы электродов. [16] |
Исследование анодного поведения меди в щелочи переменным током показало, что на кривой дифференциальной емкости электрода при потенциалах второго анодного процесса обнаруживается отчетливо выраженный максимум, на кривой сопротивления - минимум. При этом было учтено, что с увеличением частоты переменного тока емкость электрода стремится к емкости двойного электрического слоя Сл, а сопротивление - к сопротивлению адсорбции Ладо и что сопротивлением раствора можно пренебречь. [17]
Такие приборы, обладающие повышенной чувствительностью к емкости, особенно удобны для исследования дифференциальной емкости электрода, однако при измерении омических составляющих они гораздо менее точны. [18]
Такие цепи, обладающие повышенной чувствительностью к емкости, особенно пригодны для исследования дифференциальной емкости электрода, однако при измерении омических составляющих они менее точны по сравнению с переменноточнымн цепями. [19]
Таким образом, производная пограничного натяжения по потенциалу, взятая с обратным знаком, выражает дифференциальную емкость электрода, которую с большой точностью можно измерить непосредственно. [20]
С а, нас - дифференциальная емкость электрода, когда его поверхность полностью покрыта адсорбированным веществом; Cd) B - дифференциальная емкость электрода в отсутствие адсорбированного вещества; Cd - дифференциальная емкость электрода при концентрации поверхностноактивного вещества, меньшей, чем концентрация, соответствующая полному покрытию поверхности. Все значения емкостей должны быть измерены при одном и том же потенциале. [21]
С а, нас - дифференциальная емкость электрода, когда его поверхность полностью покрыта адсорбированным веществом; Cd) B - дифференциальная емкость электрода в отсутствие адсорбированного вещества; Cd - дифференциальная емкость электрода при концентрации поверхностноактивного вещества, меньшей, чем концентрация, соответствующая полному покрытию поверхности. Все значения емкостей должны быть измерены при одном и том же потенциале. [22]
Однако метод сравнения рассчитанных и экспериментальных кривых зависимости поверхностного давления от заряда электрода, как было впоследствии отмечено Парсонсом [28], является мало чувствительным к форме изотермы адсорбции. Значительно более чувствительной функцией является дифференциальная емкость электрода. АСд от Е при использовании изотерм адсорбции Генри, Фрейндлиха, Ленгмюра, Темкина и изотермы с вириаль-ными коэффициентами. Сопоставление полученных уравнений с экспериментальными данными по адсорбции на ртути молекул тиомочевины [127] и н - С5НиОН [177] показало, однако, что исследованные изотермы адсорбции лишь в первом приближении могут быть использованы для описания опытных С, Е - кривых. [23]
Для железа, характеризующегося высокой энергией связи М - Н, адсорбция галогенид-ионов приводит к замедлению реакции разряда ионов водорода. При этом перенапряжение водорода растет, а дифференциальная емкость электрода снижается. Однако при адсорбции сульфид-анионов эта закономерность нарушается: скорость разряда водорода увеличивается, перенапряжение водорода снижается, дифференциальная емкость не меняется. [24]
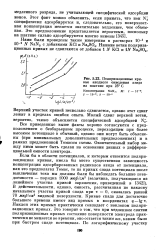 |
Поляризационные кривые анодного окисления азида на платине при 25 С. [25] |
Все приведенные выше факты хорошо согласуются с предположением о безбарьерном процессе, переходящем при более высоком потенциале в обычный, однако они могут быть объяснены ( при минимальных дополнительных предположениях) и в рамках предложенной Томасом схемы. Окончательный выбор между ними может быть сделан на основании данных о дифференциальной емкости электрода. [26]
Таким образом, Осциллографическая полярография позволяет быстро и наглядно устанавливать адсорбцию поверх-ностноактивных веществ на электроде в широкой области потенциалов. При адсорбции на электроде, которая обычно имеет место в ограниченной области потенциалов, происходит изменение дифференциальной емкости электрода, а следовательно, и тока заряжения. Потенциалу адсорбции или десорбции вещества соответствует острый максимум ( пик) на кривой ( рис. 244), обусловленный увеличением дифференциальной емкости, сопровождающим перестройку двойного электрического слоя. [28]
ИВПТ, такой эффект наблюдается. Это происходит из-за адсорбционного накопления ПАВ на необновляющейся поверхности стационарного электрода. О ходе накопления ПАВ на этой поверхности, а тем самым косвенно и о концентрации ПАВ в растворе, судят по так называемым капацитограммам - кривым зависимости дифференциальной емкости электрода от времени. Практически вместо них регистрируют аналогичные по форме кривые временной зависимости емкостной составляющей тока в ВПТ-С с ФС или тока без временной селекции в ВПТ-П и других вариантах ВПТ. При прочих равных условиях капацитограммы позволяют сопоставлять между собой площади разные электродов по значениям токов при заданном времени измерения. [29]
Для того чтобы зарядить электрод до более положительного ( отрицательного) потенциала, к нему необходимо подвести положительный ( отрицательный) заряд. Количество электричества, требуемое для заряжения электрода, зависит от его емкости. В растворах простых неорганических солей при потенциалах немного поло-жительнее потенциала нулевого заряда емкость электрода составляет - 20 мкФ / см2, а при более положительных потенциалах она выше. Емкость электрода - не постоянная величина, а в той или иной мере зависит от потенциала электрода. Чтобы учесть эту зависимость, вводят понятие дифференциальной емкости электрода С dqldE, где q - заряд электрода. Вообще говоря, емкость электрода очень высока, что обусловлено исключительно малой толщиной образующегося вблизи его поверхности молекулярного конденсатора [ ср. В подобной структуре условие электронейтральности не соблюдается, и в области двойного электрического слоя преобладают ионы определенного вида. В целом, однако, двойной электрический слой остается электронейтральным: сумма зарядов обкладок конденсатора ( в металле и в растворе) равна нулю. Такая модель двойного электрического слоя ( описанная Гельмгольцем в 1879 г.) законна, однако, лишь для довольно концентрированных растворов электролитов. В более разбавленных растворах расстояния, на которых ионы в растворе образуют обкладку двойного электрического слоя, возрастают вследствие теплового движения ионов. Теперь преобладает структура, аналогичная ионной атмосфере вокруг отдельного иона. Такая структура называется диффузным двойным слоем. На рис. 59 схематически показан двойной электрический слой на границе раздела металлический электрод / раствор электролита. [30]
Страницы: 1 2 3
