Магнитный момент - соединение
Cтраница 1
Магнитный момент соединений, содержащих ион [ NbCl5 ( OR) ] 2, соответствует одному неспаренному электрону, а соединение [ NbCl - ( ОС2Н5) зРу ] 2 диамагнитно, что свидетельствует о взаимодействии Nb - Nb. Диамагнитная четырехокись полимерна и очень легко гидролизуется. [1]
Магнитный момент соединения равен 5 47 р в; высокоспиновым является, очевидно, комплекс двухвалентного железа РепРуб ] 2, анион [ Fe4 ( CO) is ] 2 - диамагнитен. [2]
Магнитные моменты соединений второго и третьего рядов переходных элементов показывают, что эти соединения всегда спин-спаренного типа. [3]
Если учесть большой магнитный момент соединений Eu ( III), равный 3 61 магнетона Бора, то указанное расщепление можно, вероятно, отнести к расщеплению магнитным полем дважды вырожденных уровней. Такие уровни возникают при повышении симметрии окружения атома европия, если влияние атомов кислорода, связанных с атомом европия, становится преобладающим по сравнению с влиянием остальной части молекулы лиганда. [4]
Магнитный момент полностью совпадает с магнитными моментами соединений трехвалентного рутения. [5]
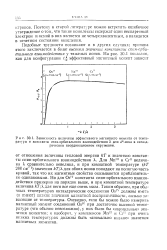 |
Зависимость величины эффективного магнитного момента от температуры и константы спин-орбитального взаимодействия X для й4 - иона в октаьд-рическом координационном окружении. [6] |
Очевидно, если бы можно было измерить магнитный момент соединений Oslv при достаточно высокой температуре ( что обычно невозможно), у них были бы нормальные значения моментов; и наоборот, у комплексов Мп П и Сг при очень низких температурах должны быть аномально низкие значения магнитных моментов. [7]
Расстояния Mo - Mo, лежащие в пределах 2 65 - 2 82 А, и расстояние W - W, равное 2 41 А, так же как и очень низкие магнитные моменты соединений Мо и W8, свидетельствуют о наличии связей металл - металл. [8]
Если, однако, заслоненная форма комплекса фиксируется мостиковыми лигандами, как это имеет место, например, в Re2 ( CeH5COO) 4Cl2 - 2CHCl3 [411], увеличение общего числа электронов ( при окислении металла или замене Re на Ru, Rh и др.) может и не вызвать изменения геометрической конфигурации комплекса. При этом, однако, магнитный момент соединения и расстояния М - М должны изменяться в соответствии с размещением лишних электронов на разрыхляющих орбиталях. [9]
Для кобальта и железа известны изонитрильные комплексы и аце-тилацетонаты. В комплексах типа [ ЭГз ( РКзЫ ( где Г - Cl, Br, a R - СН3 и др.) магнитные моменты соединений никеля соответствуют одному, а кобальта - двум непарным электронам. Темно-синий хлоридный комплекс никеля ( с R - С2Н5) плавится при 63 С, а кобальта - при 104 С. [10]
Для кобальта и железа известны изонитрильные комплексы и аце-тидацетонаты. В комплексах типа [ ЭГ3 ( РКзЬ ] ( где Г - Cl, Br, a R - СН3 и др.) магнитные моменты соединений никеля соответствуют одному, а кобальта - двум непарным электронам. Темно-синий хлоридный комплекс никеля ( с R - C2Hj) плавится при 63 С, а кобальта - при 104 С. С) типа Na3 [ Ni ( ONCHj) e ], интересное как интенсивностью своей коричневой окраски, так и окисляемостью до Na2 [ Ni ( ONCH2) e ] уже под действием кислорода воздуха. С) диамагнитно ( х - 102) и хорошб растворимо в воде, но не растворяется в органических растворителях. [11]
Предполагается структура, аналогичная бис-ацетилацето-нату Ni, в которой осуществляются тримерные молекулы с ок-таэдрическим окружением атомов Ni. Этот вывод подтверждается магнитными и спектральными данными. Магнитный момент соединения 3 28 ЦБ, следовательно, исключается квадратно-шюс-костная координация. Спектры отражения в видимой области для бис-салицилальдегидата и бис-ацетилацетоната Ni идентичны и отличны от соединений Ni с тетраэдрической координацией. [12]
Страницы: 1