Присутствие моно
Cтраница 2
Таким образом, из анализа спектра ЯМР13С можно сделать вывод о присутствии моно - или сшш-дизамещенного алленового фрагмента, моно -, ди - или тризамещенного бензольного ядра, одной или двух метальных групп. [16]
Во фракции 200 - 300 С нефти Само-тлорского месторождения среди ароматических углеводородов обнаружено присутствие моно -, ди - ( п - и ж-изомеров), три - ( 1, 2, 3 - и 1 3 5 -), тетра - ( все три типа замещения), а также пентазамещенные бензолы. [17]
На основании исследования вторичных ароматических углеводородов во фракции 200 - 300 С установлено присутствие моно - и диметилтетралинов, а также циклогексилбензолов и ди-метилциклогексилбензолов. [18]
Браун и Матисон [674] изучали скорость полимеризации стирола ( и а-метилстирола) в присутствии моно -, ди - и трихлор-уксусной кислоты в массе и в различных полярных растворителях в отсутствие воздуха. На основании полученных результатов предложен катионный механизм реакции. [19]
Конденсацию проводят при 60 С под давлением. Присутствие моно - и три-этаноламинов при нитровании диэтаноламина нежелательно вследствие получения из них нестабильных продуктов. Выделение и очистку диэтаноламина производят вакуум-разгонкой, при этом отбирают фракцию, кипящую при остаточном давлении 10 мм рт. ст. в пределах 145 - 155 С. [20]
Бензол при комнатной температуре не алкилируется пропиленом в присутствии этих кислот [51], а при 80 алкилат получается с выходом 56 % от теорет. Алкилирование бензола пропиленом в присутствии моно - и дифторфосфорных кислот, насыщенных BF3, при 20 и скорости пропускания пропилена 3 5 л / час протекает энергично с образованием высокого выхода изопропилбензола. [21]
Поэтому весьма важной операцией является их выделение из реакционной смеси. Необходимо помнить, что в мономере, поступающем на поликонденсацию, присутствие моно - и триорганохлорсиланов недопустимо. Это ведет, в конечном счете, к получению соответственно низкомолекулярного или пространственного ( трехмерного) полимера. Разделение мономеров обычно осуществляют тщательной ректификацией. [22]
При соотношении алкина и диизобутилалюминнйгидрида, равном 2: 1, основным направлением процесса может стать дпмерн-зацпя алкина. Следует отметить, что алкеннлаланы, получаемые из терминальных ацетиленов, не дпме-рпзуются в присутствии моно - и дизамещепных алкинов. [23]
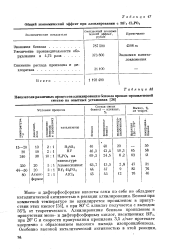 |
Общий экономический эффект при алкилированни с BFs. [24] |
Моно - и дифторфосфорные кислоты сами по себе не обладают каталитической активностью в реакции алкилирования. Бензол при комнатной температуре не алкилируется пропиленом в присутствии этих кислот [51], а при 80 С алкилат получается с выходом 56 % от теоретического. Алкилирование бензола пропиленом в присутствии моно - и дифторфосфорных кислот, насыщенных ВГз, при 20 С и скорости пропускания пропилена 3 5 л / час протекает энергично с образованием высокого выхода изопропилбензола. [25]
Гидрогенолиз узких фракций сернистых соединений проводили в этаноле с 10 - 15-кратным количеством скелетного никеля ( по весу) при температуре 80 С в течение 2 часов. Полученные алифатические и моноциклические углеводороды указывают на присутствие моно -: бициклических сульфидов. [26]
В прибор помещают каплю исследуемого раствора и каплю 20 % - ного раствора NaOH или зернышко твердого NaOH. Прибор закрывают пробкой и нагревают на водяной бане. В присутствии диметиламина немедленно, а в присутствии диэтиламина через некоторое время капля фурфурола окрашивается в желтый или оранжевый цвет. Присутствие моно - и триметил ( этил) аминов не препятствует реакции. [27]
Райл и Сэнджер [3] наблюдали, что после гидролиза инсулина холодной концентрированной НС1 получается значительно большее число цистинсодержащих пептидов, чем то, какое соответствовало бы белку, все молекулы которого имели бы одинаковую первичную структуру. Авторы пришли к заключению, что в результате разрыва дисульфидных связей происходит разрыв имевшихся и образование новых дисульфидных связей между остатками полуцистина. Это явление еще больше усложняет попытку определить, какие же из полуцистнновых остатков связаны друг с другом в исходной молекуле инсулина. Явление дисульфидного обмена можно легко показать путем растворения цистина и N, М - бис-динитрофенилцистина в смеси концентрированных соляной и уксусной кислот ( в отношении 1: 2 по объему) и выдерживания смеси в течение 3 - 4 дней при комнатной температуре. После разбавления смеси водой и удаления оставшегося бисдинитрофенилцистина путем извлечения этилаце-татом можно обнаружить присутствие моно ( динитрофенил) цистина в окрашенном водном слое. [28]
Страницы: 1 2