Моноокись - ванадий
Cтраница 1
Моноокись ванадия VO - светло-серые с металлич. Теплота образования АЯаон - - - 106 6 ккал / молъ. В воде VO нерастворима; с рааб: кислотами образует растворы бледно-голубого или фиолетового цвета, ее соли - энергичные восстановители. Моноокись может быть получена спеканием в вакууме при высоких темп-рах смеси металлич. [1]
 |
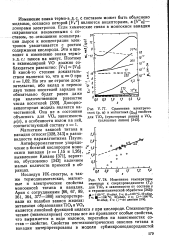
Изменение энер.| Изменения коэффициента термо-э. д. с. в зависимости от состава TiOs и VOS. [2] |
В отличие от моноокиси ванадия коэффициент а для ТЮ3 является линейной функцией состава. [3]
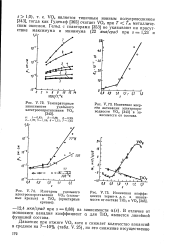
Магнитная восприимчивость хм моноокиси ванадия измерена Бэнусом и Ридом [343] при увеличении напряженности поля до 17 2 кэ ( рис. V. Как видно из рисунка, при повышенных температурах кубическая моноокись ванадия является слабым парамагнетиком во всей области составов. Увеличение % м происходит для всех измеренных составов и температур. [4]
Антиферромагнитное упорядочение в богатой кислородом моноокиси ванадия ( s 1 15 и 1 26), выявленное Кавано [371], вероятно, обусловлено [343] наличием малых количеств примесей в образцах. [6]
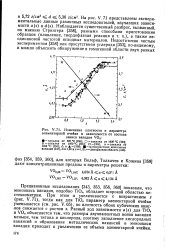 |
Изменение плотности и параметра. [7] |
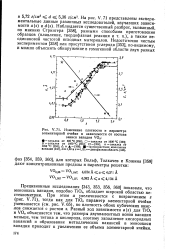
Прецизионные исследования [343, 353, 356, 360] показали, что моноокись ванадия, подобно TiOs, обладает широкой областью нестехиометрии. При этом а увеличивается с возрастанием s ( рис. V. ТЮ параметр элементарной ячейки уменьшается ( см. рис. V. Разный ход зависимости a ( s) для ТЮ8 и VOS объясняется тем, что размеры двухвалентных ионов ванадия меньше, чем титана и кислорода, поэтому заполнение кислородных вакансий и образование металлических вакансий в моноокиси ванадия приводит к увеличению ее объема элементарной ячейки. [8]
При этом в работе [24], посвященной изучению состояний электронов в моноокиси ванадия, учитывались не только двух -, но и трехцентровые интегралы. [9]
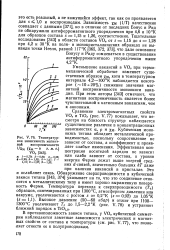 |
Температурная зависимость магнитной восприимчивости. / Хм ( Хм - в м. е. VOS. [10] |
Уменьшение вакансий в VOS при термомеханической обработке изменяет существенным образом хм, хотя в температурном интервале 4 2 - 100 К наблюдается некоторое ( - 10 - 20 %) снижение значения магнитной восприимчивости моноокиси ванадия. При этом авторы [343] отмечают, что магнитная восприимчивость является более чувствительной к катионным вакансиям, чем к анионным. [11]
Магнитная восприимчивость хм моноокиси ванадия измерена Бэнусом и Ридом [343] при увеличении напряженности поля до 17 2 кэ ( рис. V. Как видно из рисунка, при повышенных температурах кубическая моноокись ванадия является слабым парамагнетиком во всей области составов. Увеличение % м происходит для всех измеренных составов и температур. [12]
Шенберг [23] считал, что она образуется в системе тантал-кислород только как промежуточная примесная фаза, но эти наблюдения не подтвердились другими авторами. Брауер и Моравец [24 ] нашли, что моноокись ниобия образует кубические смешанные кристаллы с моноокисью ванадия. При нагревании NbO до 1700 - 2050 С в глубоком вакууме со сте-хиометрической смесью Та2О5 ЗТа, а также при нагревании в тех же условиях смесей Nb2O5 ЗТа или Та2О5 ЗМЬ образуются смешанные кристаллы типа двуокиси ( Nb, Та) О2 вместе с металлической фазой. [13]
 |
Изменение плотности и параметра. [14] |
Прецизионные исследования [343, 353, 356, 360] показали, что моноокись ванадия, подобно TiOs, обладает широкой областью нестехиометрии. При этом а увеличивается с возрастанием s ( рис. V. ТЮ параметр элементарной ячейки уменьшается ( см. рис. V. Разный ход зависимости a ( s) для ТЮ8 и VOS объясняется тем, что размеры двухвалентных ионов ванадия меньше, чем титана и кислорода, поэтому заполнение кислородных вакансий и образование металлических вакансий в моноокиси ванадия приводит к увеличению ее объема элементарной ячейки. [15]
Страницы: 1