Моноокись - титан
Cтраница 1
Моноокись титана по химическим свойствам отличается от карбида и оксикарбидов. Она устойчива в окислительных средах и менее устойчива в кислотах неокислителях. [1]
Моноокись титана образует кристаллы бронзового цвета с плотностью 4 93 г / см3, плавящиеся при 1750, растворяющиеся в разб. [2]
Нагреванием моноокиси титана выше 800 получают двуокись титана. [3]
Зиберт, Маккенна и др. Электролитическое восстановление моноокиси титана. [4]
Это хорошо иллюстрируется на примере окислов титана: заметная скорость хлорирования моноокиси титана ТЮ наблюдается при 215 С, Ti2O3 - при 225 С и ТЮ2 - только при 850 С. [5]
В настоящей работе проведено исследование поведения карбида титана, оксикарбидов с разным содержанием углерода и кислорода и моноокиси титана, а также карбида и оксикарбидов циркония разного состава в химически агрессивных средах. [6]
 |
Изменение значений периода решетки твердого раствора Т1С - - ТЮ от состава. [7] |
В соответствии с приведенной схемой отсутствие новых фазовых составляющих в твердом остатке определяется образованием по реакции а моноокиси титана с последующим ее растворением в TiC с формированием оксикарбидных соединений б, характеризующихся прогрессирующим уменьшением периода кристаллической решетки структуры NaCl с ростом составляющей ТЮ. На рис. 24 представлена зависимость изменения периода решетки твердого раствора TiC-ТЮ от состава. [8]
Сообщается о разработке в массовом производстве метода выращивания крупных монокристаллов ( длиной 305 мм и 0 19 мм) вольфрама, молибдена, ванадия, ниобия, тантала, карбида титана, моноокиси титана, полуторной окиси титана и дисилицида молибдена. Для выращивания этих монокристаллических слитков применяют метод дуговой плавки, в основе которого лежит по существу принцип, использованный в методе Вернейля для получения монокристаллических булек драгоценных камней, таких, как сапфиры и рубины. [9]
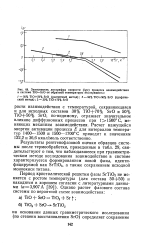 |
Зависимость логарифма скорости ( Igw процесса взаимодействия в системе TiO - SrO от обратной температуры эксперимента. [10] |
Результаты рентгенофазовой оценки образцов системы после термообработки, приведенные в табл. 29, свидетельствуют о том, что наблюдавшееся при гравиметрическом методе исследования взаимодействие в системе характеризуется формированием новой фазы, идентифицируемой как SrTiO3, а также сохранением исходной моноокиси титана. [11]
 |
Температурная зависимость магнитной восприимчивости. / Хм ( Хм - в м. е. VOS. [12] |
Кубическая моноокись титана обладает металлической проводимостью, поскольку сопротивление не зависит от состава, а коэффициент а проявляет слабые изменения. Эффективная концентрация носителей зарядов не зависит или слабо зависит от состава, а уровни энергии Ферми лежат выше энергий средних d - связей, значительно больших kT даже при наличии вакансий в кристалле. [13]
В системе TiC - МеО оксикарбидное соединение титана ( TiCxOy) формируется на основе решетки карбида титана, и концентрация кислорода в нем увеличивается с ростом температуры. Указанная особенность взаимодействия подтверждается результатами исследований авторов и предполагает образование моноокиси титана и последующее ее растворение в карбиде. Эти результаты согласуются с выводами работы [16], в которой отмечалось образование оксикарбидных фаз в процессе взаимодействия в системе TiC-MgO, и противоречат результатам работы [9], автор которой не обнаружил следов взаимодействия в системе TiC - А12Оз при 1900 С. [14]
В некоторых количествах титан производят восстановлением двуокиси титана. При выборе восстановителя для двуокиси титана необходимо учитывать, что восстановление протекает через стадию образования низшего окисла TiO ( моноокись титана), обладающего высокой химической прочностью. [15]
Страницы: 1 2