Моносульфид - железо
Cтраница 1
Моносульфид железа растворим в кислотах, за исключением азотной. [1]
Чистый моносульфид железа получают из чистого восстановленного железа и перегнанной серы. Стехиометрические количества железа и серы нагревают в высокоэвакуированной кварцевой трубке в течение 24 ч до 1000 С. [2]
Сернистое железо ( моносульфид железа) FeS - черные кристаллы с металлич. FeS образуется при нагревании железа с серой; выпадает также при прибавлении ( NII4) 2S к р-рам солей Fe ( II) в виде черного осадка, практически нерастворимого в воде, но легко растворимого в разб. Продажное сернистое железо ( всегда содержащее небольшой избыток Fe) служит для получения сероводорода. [3]
Сернистое железо ( моносульфид железа) FeS - черные кристаллы с металлич. Теплота образования A / / 9s - 22 72 ккал / молъ. FeS образуется при нагревании железа с серой; выпадает также при прибавлении ( NH4) 2S к р-рам солей Fe ( II) в виде черного осадка, практически нерастворимого в воде, но легко растворимого в разб. Продажное сернистое железо ( всегда содержащее небольшой избыток Fe) служит для получения сероводорода. [4]
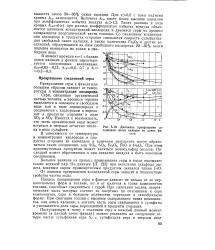 |
Динамика превращения соединений окиси кальция по длине факела. [5] |
При этом: промежуточным ( продуктом может являться моносульфид железа. Последний может образоваться три нехватке воздуха и быть конечным соединением. [6]
Имеются лишь указания [59], что присутствующий в метеоритах моносульфид железа имеет формулу, близкую к FeS. Наблюдения ряда авторов ( см., например, [109]) показывают далее, что остаток от прокаливания пирита, как правило, содержит более 50 атомных процентов серы. [7]
 |
Зависимость глубины коррозии сталей Т22 и ТР321 за 120 ч от температуры под AS MM влиянием комплексных сульфатов. [8] |
На поверхности трубы комплексные сульфаты реагируют с чистым металлом с образованием простого сульфата и моносульфида железа. [9]
Окисление сульфидов перекисью водорода в спиртовой среде, подавляющей диссоциацию, сопровождается образованием сульфатов железа. Когда окисляется моносульфид железа ( FeS), то при сохранении соотношения железа и серы 1: 1 может образоваться только Fe ( OH) SO4 [ 2FeS 9H2O2 2Fe ( OH) SO4 8H2O ], основная соль, покрывающая поверхность зерен моносульфида пленкой, защищающей их от дальнейшего окисления. Это - соль, растворимая в водно-спиртовой среде и не мешающая дальнейшему окислению дисульфида железа. [10]
Несоответствие данных по эффективности действия дисульфида молибдена связано, по-видимому, с влиянием на его активность дисперсионной среды и возможных химических реакций с компонентами смазок ( прежде всего с присадками) и металлическими поверхностями. О химическом взаимодействии Mo S2 со сталью трущейся пары с образованием моносульфида железа впервые сообщено в работе [54], в которой отмечалось, что для промежуточного образования сероводорода необходима вода. В дальнейшем показано, что химическая реакция между дисульфидом молибдена и железным порошком происходит и в отсутствии водяного пара при 700 - 730 С. Однако необходимо учитывать и возможные реакции MoS2 с различными оксидами железа или нитрилом железа. При определенных условиях с дисульфидом молибдена могут взаимодействовать присутствующие в легированных сталях элементы. [11]
Продукты реакции находятся в растворе, так как бромид желе-за ( Ш) и элементарная сера растворимы в спиртовом растворе брома. Сульфиды железа при окислении бромом в спиртовой среде переходят в раствор в соответствии с их растворимостью: в первую очередь более растворимый моносульфид железа, затем менее растворимый дисульфид железа. [12]
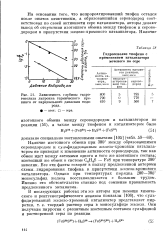 |
Зависимость глубины гидро-генолиза лигроина термического крекинга от парциального давления водорода. [13] |
Наличие изотопного обмена при 300 между образовавшимся сероводородом и сульфидированным железо-хромовым катализатором не приводит к изменению активности сероводорода, так как обмен идет между автомами одного и того же изотопного состава; изотопный же обмен в системе C4H4S - FeS при температуре 300 невелик. Однако при температурах порядка 200 - 300 моносульфид железа восстанавливается с большим трудом. Именно это обстоятельство ставило под сомнение правильность предложенного механизма. [14]
Как и следовало ожидать, сульфид железа, имея наибольшую ( на приведенных металлов) растворимость, практически из кислых растворов не осаждается. Химический анализ пробы сульфида, высушенный в эксикаторе над хлористым кальцием при комнатной температуре, указал на соотношение железа к сере, соответствующее дисульфиду железа. Стало очевидным, что активное газовыделение из раствора после освобождения системы от давления сероводорода, по-видимому, обусловливалось обратным процессом растворения образующегося в условиях опыта моносульфида железа и, возможно, других, легко растворимых в кислоте сернистых соединений типа пирротина. [15]
Страницы: 1