Железо - гем
Cтраница 1
Железо гемов может находиться в окисленном или восстановленном состоянии и образуег координац. В зависимости от белкового окружения гемы различаются по св-вам: один ( гем а), высокоспиновый, после восстановления реагирует с О2 или СО, СМ. Другой ( гем а), низкоспиновый, в такие р-ции не вступает. Один из них, СиА, дает сигнал в спектре ЭПР и взаимод. Сив, не дает сигналов, взаимод. Эти субъединицы играют главную роль в выполнении биол. [1]
 |
Механизм гидроксилирования ксенобиотиков микросомальными монооксигеназами. SH - восстановленный субстрат. [2] |
Связывание субстратов второго типа происходит с шестой координационной связью железа гема, что индуцирует переход из высокоспинового в низкоспиновое состояние. [3]
В процессе катаболизма гемоглобина его белковый компонент ( глобин) гидролизуется до аминокислот; железо гема включается в общий пул железа в организме и может вновь использоваться. Вместе с тем свободная от железа порфириновая часть гема необратимо расщепляется до образования желчных пигментов, которые выводятся из организма с содержимым толстого кишечника. Таким образом, гем и продукты его распада не могут реутилизироваться в процессе синтеза порфириновой структуры гемопротеинов. Синтез сложного тетрапиррольного комплекса происходит в организме de novo из простых предшественников. [4]
 |
Локализация ферментов. [5] |
В ряде случаев электрон с цитохрома Ь5 поступает на цитохром Р-450 и участвует в восстановлении железа гема. НАДФН-зависимый флавопротеин представляет собой димер с молекулярной массой 40 5 kDa, причем каждая субъединица содержит 1 молекулу ФАД. [6]
В ряде случаев электрон с цитохрома Ъ5 поступает на цитохром р450 и участвует в восстановлении железа гема. [7]
Хотя это нельзя еще считать окончательно установленным, все же большинство авторов придерживается того мнения, что в гемоглобине железо гема соединено с имидазольной группировкой гистидина. [8]
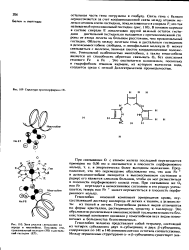 |
Структура протопорфирина IX.| Зона участка связывания кл лоро да в миоглоби не. Пока за ны гем, проксимальный гистидин ( F8 и днстальный гистидин ( Е7. [9] |
В гемовом кармане в составе спирали Е локализован другой важный остаток гистидина днстальный гистидин; он находится с противоположной сто роны от атома железа на большем расстоянии, чем проксимальный гистидин. Область между железом гема н днстальным гистидином в дезоксимиоглобине свободна, н лилофильная молекула О может связываться с железом, занимая шестое координационное положение. Это оказывается возможным, поскольку в гидрофобном гемовом кармане, из которого вытеснена вода, создается среда с низкой Диэлектрической проницаемостью. [10]
 |
Четвертичная структура. [11] |
В форме Т ( от английского tense) гемы расположены в узких карманах глобулы и присоединение кислорода затруднено. В форме R ( от английского rapid) атомы железа гема открыты и присоединение кислорода облегчается. [12]
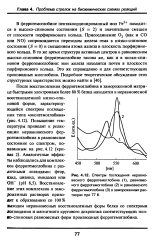 |
Спектры поглощения неравновесного феррогемоглобина ( 1, равновесного феррогемоглобина ( 2 и равновесного ферригемоглобина ( 3 в замороженных растворах при 77 К. [13] |
В феррогемоглобине пентакоординированный ион Fe2 находится в высоко-спиновом состоянии ( 5 2) и значительно смещен от плоскости порфиринового кольца. Присоединение О2 ( как и СО или NO) сопровождается переходом железа гема в низко-спиновое состояние ( 5 0) и смещением атома железа в плоскость порфиринового кольца. В то же время структура активных центров в равновесном высоко-спиновом ферригемоглобине такова же, как и в низко-спиновом феррогемоглобине: ион железа находится почти в плоскости порфиринового кольца. Это же справедливо и для соответствующих производных миоглобина. [14]
Реакции микросомального окисления катализируются НАДФН - и НАДН-зависимыми ферментными системами в присутствии кислорода. НАДФН-зависимый флавопротеин переносит электрон от восстановленного НАДФН на терминальный фермент - цитохром Р-450, восстанавливая железо гема последнего. [15]
Страницы: 1 2