Надперекись - натрий
Cтраница 2
В области температур от - [ - 10 до - 10 С надперекиси натрия и калия взаимодействуют с водяным паром и углекислым газом с выделением только надперекисного кислорода и образованием пероксодикарбо-натов Na и К. Образование последних идет через гидраты перекисей. Термической устойчивостью гидратов перекисей определяется верхний температурный предел образования пероксодикарбонатов при действии углекислого газа на надперекиси. [16]
Для проверки этого предположения октагидрат перекиси натрия был синтезирован нами из перекиси натрия, надперекиси натрия и действием перекиси водорода на насыщенный раствор гидроокиси натрия при 0 С. [17]
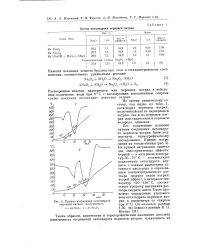 |
Кривые нагревания октагидрата перекиси натрия, полученного. [18] |
По своему химическому составу, как видно из табл. 1, октагидрат перекиси натрия, полученный как из надперекиси натрия, так и из перекиси натрия или гидроокиси и перекиси водорода, одинаков. [19]
В некоторых случаях кислород выделяют из перекиси натрия Na2O2 или из перекиси калия К2О2, а также из надперекиси натрия Na2O4, воздействуя на них парами воды в присутствии двуокиси углерода. Из 1 кг перекиси калия получается 90 - 100 дм3, а из I кг перекиси натрия до 140 дм3 кислорода. [20]
В некоторых случаях кислород выделяют из перекиси натрия Na2O2 или из перекиси калия К2О2, а также из надперекиси натрия Na2O4, воздействуя на них парами воды в присутствии двуокиси углерода. Из 1 кг перекиси калия получается 90 - 100 дм3, а из 1 кг перекиси натрия до 140 дм3 кислорода. [21]
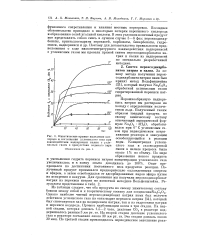 |
Кинетические кривые выделения кислорода и поглощения углекислого газа при взаимодействии надперекиси калия с углекислым газом в присутствии водяного пара. [22] |
Однако наиболее чистый пероксодикарбонат натрия нами был получен действием углекислого газа на октагидрат перекиси натрия [34], который был синтезирован как из надперекиси натрия, так и из гидроокиси натрия и перекиси водорода. [23]
В частности, почти не изучены реакции надперекисей натрия и калия с водяным паром и углекислым газом. [24]
Перекись ( или пероксид) натрия Na2O2 образуется при сжигании натрия на воздухе или в кислороде. Получающийся продукт имеет слабо-желтоватую окраску, обусловленную примесью соединения NaO2, называемого надперекисью натрия. [25]
В нашей стране в послевоенный период достигнуты значительны успехи и в научной, и в прикладной области. Достаточно здесь напомнить о работах И. А. Казарновского по синтезу, изучению свойств и реакционной способности надперекиси натрия и нового класса перекисных соединений - неорганических озонидов, об исследованиях А. И. Бродского, впервые применившего тяжелый изотоп кислорода для выяснения механизма образования и распада перекисных соединений, о систематических исследованиях М. И. Гуревич по установлению природы перекисных соединений урана, об исследованиях Н. И. Кобозева по синтезу перекиси водорода в электроразряде, об исследованиях Г. А. Богданова по механизму каталитического разложения перекиси водорода, о систематических исследованиях С. Макарова с сотрудниками взаимодействия перекиси водорода с гидратами окислов и солями, позволивших разработать рациональные способы синтеза ряда перекисных соединений. [26]
Третий период характеризуется более глубокими как в СССР, так ж за рубежом, исследованиями строения, свойств и характера связи в пе-рекисных соединениях. К этому периоду относятся работы И. А. Казарновского и сотрудников по изучению структуры ряда перекисных соединений, открытие ими надперекиси натрия, фундаментальные исследования школы канадского ученого О. [27]
Надперекиси отличаются от соответствующих перекисей легкостью выделения кислорода при введении в воду с температурой льда. В аналогичных условиях в отсутствие катализатора перекиси не разлагаются. Надперекись натрия, по-видимому, устойчива лишь при низких температурах. [28]
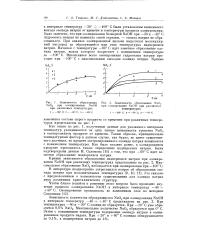 |
Зависимость образования ПРИ озонировании NaOH при различных температурах. - - - - - 100 С. г - - - - - 80 С. 3 - - - - - 60 С.| Зависимость образования NaOg. [29] |
Как видно из рис. 1, полученные данные для указанного интервала температур укладываются на одну линию зависимости процента Na03 в озонированном продукте от времени. Таким образом, принципиально температурный фактор в данном случае, как будто, не имеет существенного значения, но процент экстрагированного озонида натрия повышается с понижением температуры. Как было сказано ранее, в озонированном продукте проводилось также определение надперекиси натрия. Были подтверждены данные И. Соломона [11] о том, что при - 60 С идет заметное образование надперекиси натрия. [30]
Страницы: 1 2 3