Наклон - кривая - равновесие
Cтраница 1
Наклон кривой равновесия увеличивается с повышением температуры и уменьшением давления, так как в этом случае константа равновесия К возрастает. При этом уменьшается расход гаяа на отпаривание. [1]
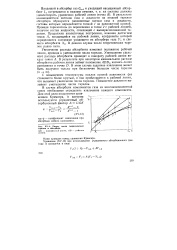 |
Расчет числа теоретических тарелок в абсорбере. [2] |
С повышением температуры наклон кривой равновесия фаз становится более крутым, и она приближается к рабочей линии, что вызывает увеличение числа тарелок. Повышение давления вызывает уменьшение числа тарелок. [3]
Таким образом, для определения наклона кривой равновесия реакции на диаграмме Т - р необходимо знание полного теплового и объемного эффектов реакции. Как мы упоминали, температура равновесия реакций с поглощением одной воды не обнаруживает заметной зависимости от глубинности, что указывает на незначительный объемный эффект таких реакций: парциальный объем воды в метаморфизующих растворах, очевидно, близок к парциальному объему воды в минералах. Линии равновесия таких реакций на диаграмме Т - р идут в первом приближении параллельно оси давлений. Эти кривые равновесия имеют вид парабол, по мере увеличения давления выполаживаю-щихся. Для более сложных реакций, при которых углекислота поглощается, а вода выделяется, предсказание знаков теплового и объемного эффекта при метаморфизме становится еще более трудным, так как мы не знаем точно состояния воды и углекислоты в природных растворах. Здесь приходится в большей степени основываться на наблюдениях минерального состава горных пород. [4]
Связь между этими скачками и наклоном кривой равновесия в точке перехода определяется уравнениями Эренфеста. [5]
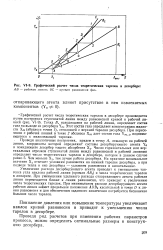 |
Графический расчет числа теоретических тарелок в десорбере. [6] |
Понижение давления или повышение температуры увеличивает наклон кривой равновесия и приводит к уменьшению числа тарелок в десорбере. [7]
При понижении давления или повышении температуры наклон кривой равновесия становится более крутым, она удаляется от рабочей линии, и число тарелок уменьшается. Если десорбция осуществляется за счет подвода тепла QB в низ десорбера, то стекающая с первой тарелки жидкость будет направляться в кипятильник ( см. гл. [8]
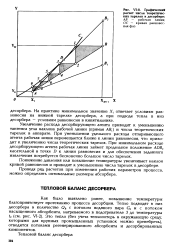 |
Графический расчет числа теоретических тарелок в десорбере. [9] |
Понижение давления или повышение температуры увеличивает наклон кривой равновесия и приводит к уменьшению числа тарелок в десорбере. [10]
В уравнениях ( 4 - 6) предполагается, что наклон кривой равновесия т я наклон рабочей линии LJ G постоянны в диапазоне рассматриваемых композиций. [11]
Величина т, входящая в это уравнение, равна среднему значению угла наклона кривой равновесия в заданных пределах перегонки. Прочие величины, входящие в уравнения ( 348) и - ( 349), известны из предыдущего. Найденная высота h3 умножается на число ступеней концентрации, которое определяется по методу, изложенному в гл. [12]
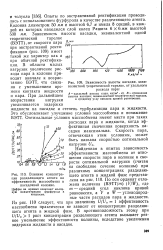 |
Влияние концентра. [13] |
По оси ординат отложена величина ( ВЭТТ / m) ( V / W), где т - средний угол наклона кривой равновесия, а V и W - углеводородные части расходов пара и жидкости. [14]
Здесь Ren - критерий Рейнольдса для пара; рж, рп - плотности жидкой и паровой фаз; т - тангенс угла наклона кривой равновесия. [15]
Страницы: 1 2