Наклон - прямая линия
Cтраница 2
Наклон лучших прямых линий делится на их стандартную ошибку, и чем больше будет это отношение, тем лучше данная прямая линия будет соответствовать опыту. После этого сразу находится наиболее вероятный порядок реакции. [16]
Угол наклона прямых линий в штриховке должен равняться 45; допускается брать этот угол равным 30 или 60 в случае, когда линии штриховки при угле 45 оказались бы параллельными линии контура ( фиг. [17]
Из наклона прямой линии находят / См / Ут. [19]
 |
Обозначения при штриховке. [20] |
Угол наклона прямых линий в штриховке должен равняться 45; допускается брать угол равным 30 или 60 в случае, когда линии штриховки при угле 45 окажутся параллельными линии контура ( фиг. [21]
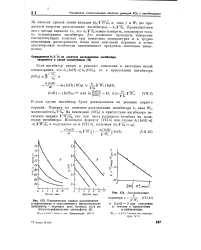 |
Кинетические кривые расходования. [22] |
По наклону прямой линии находим fk4 / yWik8 и, зная / и Wi ( по предельной скорости расходования ингибитора), - / с7 / ] КА6. Преимуществом этого метода является то, что / с. Это позволяет проводить измерения соответствующих констант при невысоких температурах и в трудно окисляемых растворителях, когда цепи окисления короткие и точно анализировать количества накопившихся продуктов окисления невозможно. [23]
По наклону прямой линии, изображающей графически зависимость одной из этих величин от времени, можно вычислить константу скорости бимолекулярной реакции. [24]
По наклону прямой линии находим fk [ YWiku и, зная / и Wi ( по предельной скорости расходования ингибитора) - k / Yke. Преимуществом этого метода является то, что k7 / Yks можно измерять, анализируя только концентрацию ингибитора. Это позволяет проводить измерения соответствующих констант при невысоких температурах и в трудно окисляемых растворителях, когда цепи окисления короткие и точно анализировать количества накопившихся продуктов окисления невозможно. [25]
По наклону прямых линий, получаемых при графическом изображении экспериментальных данных в координатах 1 / [ AJ, t или l / x, l / t, может быть рассчитана константа скорости реакции. [26]
 |
Кинетика взаимодействия lj с р-фенилпропиоловой кислотой. [27] |
По наклону прямых линий, получаемых при графическом изображении экспериментальных данных в координатах 1 / IA ], t или Их, lt, может быть рассчитана константа скорости реакции. [28]
Угловой коэффициент наклона прямой линии, изображающей эту зависимость для серии кинетических кривых, отвечающих разным [ Ai ] o, дает непосредственно величину суммарного порядка реакции. [29]
В этом случае наклон прямой линии, полученной при нанесении значений критических концентраций двухвалентных катионов, соответствующих концентрации полимера, дает степень связывания, в то время как отрезок оси абсцисс, отсекаемый этой прямой, дает концентрацию свободных - несвязанных - катионов. При сравнении эффекта добавки различных катионов найдено, что осаждение достигается при одной и той же степени связывания, независимо от характера двухвалентного катиона. [30]
Страницы: 1 2 3 4 5