Наклон - полулогарифмическая прямая
Cтраница 1
 |
Схема кулонометрии при постоянной силе тока. [1] |
Наклон полулогарифмической прямой можно определить по нескольким точкам, соответствующим силе тока в начальный период электролиза; это дает возможность вычислить Q, не доводя электролиз до самого конца. [2]
Пстоянную распада можно определить графически через тангенс угла наклона полулогарифмической прямой к оси абсцисс. [3]
По измерениям Баудена ( 1930), относящимся к разбавленным растворам серной кислоты, рост температуры снижает кислород-нос перенапряжение на платине за счет уменьшения величины а: наклон полулогарифмических прямых, наоборот, увеличивается. При заданной температуре наклон является функцией концентрации кислоты и растет параллельно с ней. [4]
 |
Поляризационные кривые при. [5] |
По измерениям Баудена ( 1930), относящимся к разбавленным растворам серной кислоты, рост температуры снижает кислородное перенапряжение на платине за счет уменьшения величины а: наклон полулогарифмических прямых, наоборот, увеличивается. При заданной температуре наклон является функцией концентрации кислоты и растет параллельно с ней. [6]
 |
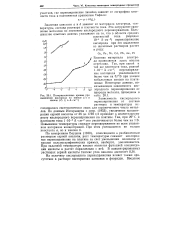
Поляризационные кривые при выделении кислорода на никеле ( / и свинце ( 2. [7] |
По измерениям Баудена ( 1930), относящимся к разбавленным растворам серной кислоты, рост температуры снижает кислородное перенапряжение на платине за счет уменьшения величины а; наклон полулогарифмических прямых, напротив, увеличивается. При заданной температуре величина наклона является функцией концентрации кислоты и растет параллельно с ней. [8]
По измерениям Баудена ( 1930), относящимся к разбавленным растворам серной кислоты, рост температуры снижает кислородное перенапряжение на платине за счет уменьшения величины а: наклон полулогарифмических прямых, наоборот, увеличивается. При заданной температуре величина наклона является - функцией концентрации кислоты и растет параллельно с ней. На величину кислородного перенапряжения влияет также присутствие в растворе посторонних катионов и фторидов. Введение добавок увеличивает кислородное перенапряжение. [9]
Реакцию проводят в термостатированном сосуде, измеряют оптическую плотность и строят график в координатах: время - логарифм оптической плотности. Определяют тангенс угла наклона прямой к оси абсцисс и по графику: концентрация хрома - тангенс угла наклона полулогарифмической прямой находят содержание хрома в растворе. [10]
Любая из стадий каждого из четырех вариантов может быть замедленной и определять скорость всей реакции. Чтобы сделать выбор между этими теоретически возможными случаями и установить действительные причины кислородного перенапряжения, следует воспользоваться критериями, вытекающими из общей теории кинетики электродных процессов. Одним из таких критериев может служить величина наклона полулогарифмических прямых. [11]
Любая из стадий каждого из четырех вариантов может быть замедленной и определять собой скорость всей реакции. Чтобы сделать выбор между этими теоретически возможными случаями и установить действительные причины кислородного перенапряжения, следует воспользоваться определенными критериями подобно тому, как это делалось при рассмотрении водородного перенапряжения. Одним из таких критериев может служить величина наклона полулогарифмических прямых. [12]
Любая из стадий каждого из четырех вариантов может быть замедленной и определять скорость всей реакции. Чтобы сделать выбор между этими теоретически возможными случаями и установить действительные причины кислородного перенапряжения, следует воспользоваться критериями, вытекающими из общей теории кинетики электродных процессов. Одним из таких критериев может служить величина наклона полулогарифмических прямых. [13]
Другие реакции, среди которых следует в первую очередь назвать выделение кислорода [ см., например, ( XIV, 9) и ( XIV, 10) ], безусловно идут с высоким перенапряжением. В практике электролиза такие реакции встречаются не реже, чем реакция электролитического выделения водорода, но изучены они гораздо слабее. Для них также характерна логарифмическая зависимость перенапряжения от ( плотности тока. Однако воспроизводится эта зависимость значительно хуже и угол наклона соответствующих полулогарифмических прямых не остается постоянным в таких широких пределах изменения плотности тока, как в случае выделения водорода. Связано это, по-видимому, с тем, что при потенциалах протекания реакций с выделением кислорода поверхность металлических электродов в той или иной мере окислена, а перенапряжение сильно зависит от степени окисления. [14]
Страницы: 1