Наклон - участок - кривая
Cтраница 1
Наклон примесного участка кривой зависит от концентрации примесей. [1]
Приведены значения tt ( экспериментальный период индукции) и ke ( тангенс угла наклона квазипрямолинейного участка кривой, изображающей зависимость степени превращения от времени), суммирующие протекание частичного восстановления при 206 5 С образцов, использованных в экспериментах, результаты которых изображены на рис. 7.11. Указаны также значения ke, измеренные при переменных температурах во второй части каждого эксперимента. [2]
 |
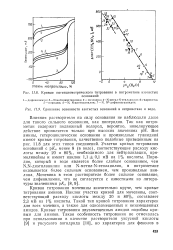
Кривые потенциометрического титрования в нитрэметане азотистых.| Сравнение основности азотистых оснований в нитрометане и воде. [3] |
Кривая титрования мочевины значительно круче, чем кривые титрования аминов. Наклон участка кривой для мочевины, соответствующий расходу кислоты между 20 и 80 %, составляет 2 3 мВ на 1 ] % кислоты. Такой тип кривой титрования характерен для всех мочевин, а также для однозамещенных и незамещенных амидов. Кривые титрования двузамещенных амидов подобны кривым для аминов. [4]
 |
Кривые потенциометрического титрования в нитрэметане азотистых.| Сравнение основности азотистых оснований в нитрометане и воде. [5] |
Кривая титрования мочевины значительно круче, чем кривые титрования аминов. Наклон участка кривой для мочевины, соответствующий расходу кислоты между 20 и 80 %, составляет 2 3 мВ на 1 % кислоты. Такой тип кривой титрования характерен для всех мочевин, а также для однозамещенных и незамещенных амидов. Кривые титрования двузамещенных амидов подобны кривым для аминов. [6]
С увеличением количества пробы минимум на кривой зависимости Нр р ( и) становится менее явно выраженным. Наклон участка кривой, отвечающего скоростям газового потока, при которых величина Нр определяется в основном составляющей, связанной с сопротивлением массопередаче, несколько убывает с увеличением нагрузки. [7]
Малый угол наклона прямой АВ ( см. рис. III.39) свидетельствует о небольшом значении теплоты физической адсорбции кислорода на гопкалите. Из угла наклона участка кривой CD этого же рисунка была определена теплота обратимой активированной адсорбции, которая оказалась равной 10 ккал / молъ. Авторы, правда, справедливо подчеркивают чисто-оценочный характер этой величины, поскольку полностью обратимым процесс активированной адсорбции становится лишь в конце ниспадающей ветви CD и поэтому, строго говоря, найденное значение ( 10 ккал) не является достаточно точной величиной, характеризующей равновесный процесс. [8]
Полученные результаты объясняются изменением характера кривых титрования при переходе от более сильных кислот к более слабым. При таком переходе все время уменьшается скачок рН и увеличивается наклон участка кривой вблизи точки эквивалентности по отношению к оси ординат, эти участки становятся все более пологими. Вследствие возрастания наклона одинаковые отклонения рТ индикаторов от рН точки эквивалентности обусловливают появление все больших погрешностей определения. [9]
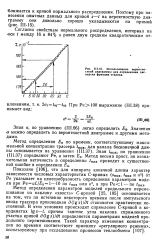 |
Использование вероятностной диаграммы для определения дисперсии функции отклика. [10] |
Метод определения параметров моделей продольного перемешивания по наклону хвоста С-кривой [25, 105] основывается на том, что по истечении некоторого времени после импульсного ввода трассера производная d ( gs) / dt становится практически постоянной. В этих условиях происходит спрямление С-кривой в координатах Igs - /, причем тангенс угла наклона спрямленного участка кривой d ( gs) / dt определяется параметрами моделей продольного перемешивания. [11]
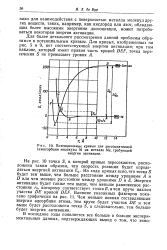 |
Потенциальные кривые для диссоциативной. [12] |
На рис. 10 точка 5, в которой кривые пересекаются, расположена таким образом, что скорость реакции будет определяться энергией активации Еа. Энергия активации будет также тем выше, чем меньше равновесное расстояние г0, которому соответствует точка Е, и чем круче наклон участка DE кривой DEF. Чем меньше ионная составляющая энергии адсорбции атома, тем круче будет участок DE и тем выше будет расположена точка S, а следовательно, тем больше будет энергия активации. [13]
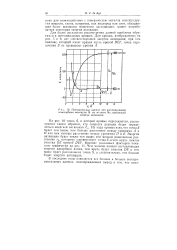 |
Потенциальные кривые для диссоциативной. [14] |
На рис. 10 точка S, в которой кривые пересекаются, расположена таким образом, что скорость реакции будет определяться энергией активации Еа. Энергия активации будет также тем выше, чем меньше равновесное расстояние г0, которому соответствует точка Е, и чем круче наклон участка DE кривой DEF. Влияние указанных факторов показано графически на рис. И. Чем меньше ионная составляющая энергии адсорбции атома, тем круче будет участок DE и тем выше будет расположена точка S, а следовательно, тем больше будет энергия активации. [15]
Страницы: 1