Накопление - серная кислота
Cтраница 1
Накопление серной кислоты в танках и других сосудах для хранения и перевозки жидкого хлора вызывает необходимость периодического удаления из них хлора и очистки от кислоты. Поскольку серная кислота находится в жидком хлоре в виде отдельного слоя, методика отбора пробы жидкого С12 на определение содержания в нем H2SO4 регламентирована. [1]
Эффект накопления серной кислоты обусловливает гораздо большее снижение активности угля по сероуглероду по сравнению с эффектом накопления элементарной серы. [2]
Основной трудностью применения сульфатного электролита с нерастворимым анодом является накопление серной кислоты в растворе, а это мешает получению никеля на катоде. В хлористых же электролитах кислотный агент - хлор - выходит из сферы электролиза и длительный электролиз с нерастворимым анодом становится принципиально возможным. [3]
При регенерации в электролизере с диафрагмой в анодном прост-транстве происходит накопление серной кислоты. Это приводит в некоторых случаях к нежелательным явлениям при использовании регенерированного раствора в качестве окислителя. Кроме того, с повышением концентрации серной кислоты падает выход бихромата при регенерации. [4]
Поскольку при образовании серной кислоты по приведенной выше реакции расходуется одна молекула воды, а серная кислота остается в фазе катионита, вначале может произойти уменьшение массы смолы вследствие удаления избытка воды с последующим увеличением массы за счет участия воды в образовании и накоплении серной кислоты. [5]
Накопление в почве токсичных и канцерогенных соединений, в том числе ртути, свинца, кадмия, цинка, радиоактивных нуклидов, бензопирена; накопление обменного натрия, соды и развитие вторичной щелочности ( кстати, последние процессы характерны для почв городской и пригородной территории г. Якутска); накопление вторичной серной кислоты в результате ее поступления с кислотными осадками или из отходов сульфидов горного производства и, как следствие, выщелачивание из субстрата и вторичное накопление в почве водорода и алюминия. [6]
Из примесей, которые могут присутствовать в жидком хлоре, примесь серной кислоты наиболее вероятна, так как всюду применяется осушка хлора серной кислотой, а методы очистки электролитического хлора от H2SO4 недостаточно совершенны. При многократном использовании этих сосудов под налип жидкого хлора серная кислота накапливается в них в таких количествах, что занимает заметную часть объема хранилищ. Накопление серной кислоты может привести к их коррозии вследствие увлажнения H2SO4 при контакте с воздухом в процессе опорожнения и последующего заполнения сосудов. По этой же причине при передавливании хлора на испарение происходит обогащение испаренного хлора примесями серной кислоты, что вызывает осложнения в производстве органических хлоропродуктов. [7]
Однако растерие своей поглотительной деятельностью постоянно смещает это равновесие, ибо корни поглощают гораздо больше гидрата окиси аммония, чем серно. Поэтому-то и происходит накопление серной кислоты в почвенном растворе и его подкисление. [8]
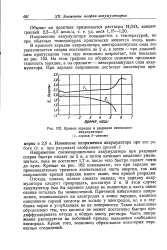 |
Кривые зарядки и разрядки свинцового аккумулятора. [9] |
Отсюда, однако, нельзя сделать вывода, что зарядку аккумулятора следует прекращать, достигнув 2 в. В этом случае аккумулятор был бы заряжен далеко не полностью и часть окиси свинца осталась бы неокисленной. Причиной избыточного напряжения, возникающего на электродах в конце зарядки, является накопление серной кислоты не только у электродов, но и в глубоких порах и углублениях на их поверхности. Такое накопление обусловлено тем, что кислота не может достаточно быстро про-диффундировать оттуда в общую массу раствора. Часть напряжения расходуется на побочный процесс выделения свободного кислорода. Кроме того, возможно образование некоторых пере-кисных соединений. [10]
Окисление восстановленных соединений серы до сульфатов, осуществляемое этими бактериями, приводит к подкислению окружающей среды, что может иметь положительные и отрицательные последствия. Подкисление почвы приводит к переводу некоторых соединений, например фосфатов, в растворимую форму, что делает их доступными для растений. Окисление нерастворимых сульфидных минералов, сопровождающееся переводом металлов в растворимую форму, облегчает их добычу. Однако накопление серной кислоты в результате деятельности этих бактерий может приводить к порче и разрушению различных сооружений. [11]
Медленная струя воздуха направляется в разбавленный раствор перекиси водорода в ячейке для измерения электропроводности. При этом не только поглощается газ, но струя воздуха вызывает быструю микроциркуляцию, которая обеспечивает тщательное перемешивание электролита, тем временем перекись водорода окисляет сернистый газ до серной кислоты. Прибор снабжен резервуаром, из которого медленно капает электролит; из резервуара периодически при помощи сифона раствор сливается в ячейку для удаления старого раствора и введения свежего электролита. При этом каждый раз сопротивление ячейки резко возрастает до большой величины, которая затем постепенно уменьшается в соответствии со скоростью накопления серной кислоты. Ячейка соединена с мостиковым осциллятором Вина, выходной импульс которого подается на самописец. [12]
Страницы: 1