Накопление - продукт - окисление
Cтраница 3
В табл. 80 приведены значения максимальных скоростей накопления продуктов окисления Wi и W2 при 145 С и давлении 50 атм в стальном реакторе для двух серий опытов - окисления бутана в жидкой фазе и окисления в газовой фазе при концентрации бутана в 6 5 раз меньшей, чем плотность бутана в жидкой фазе в данных условиях. [31]
Скорость окисления измеряется по поглощению кислорода или по накоплению продуктов окисления. [32]
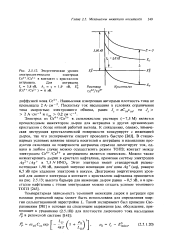 |
Энергетические уровни электролитического электрода. [33] |
В стационарных условиях влияние захвата носителей в антрацене и накопление продуктов окисления на поверхности антрацена серьезно лимитирует ток, однако в любом случае можно осуществлять режим ТОПЗ; контакт между электродом Се4 / Се3 и антраценом является омическим. Этот электрод имеет стандартный редокс-потенциал 1 98 эВ, дающий энергию ионизации для иона / 4g ( aq), равную 6 5 эВ при удалении электрона в вакуум. [34]
На рис. 210 приведены кинетические кривые расходования бутана и накопления продуктов окисления при добавках к исходному бутану различных количеств смолы, выделенной из смеси продуктов, полученной в предыдущих опытах. Добавки смолы увеличивают период индукции, снижают скорость реакции и значительно уменьшают максимальную глубину превращения бутана. При этом соответственно уменьшаются также скорости накопления и максимальные выходы продуктов окисления. [35]
В работе [13] был проведен также теоретический расчет кинетики накопления продуктов окисления по цепной схеме с учетом вырожденного разветвления на гидроперекисях и распада последних на кетоны, а их, в свою очередь, на кислоты по реакциям первого порядка. [36]
На рис. 1 представлены результаты действия р-нафтола на кинетику накопления продуктов окисления изопропилового спирта. [37]
На рис. 1 представлены результаты действия р-нафтола на кинетику накопления продуктов окисления изопропилового спирта. [38]
Учитывая тот факт, что в ходе окисления с накоплением продуктов окисления из-за изменения состава радикалов изменяется средняя активность радикалов, ведущих окисление, легко объяснить торможение реакции при введении ингибитора в исходный углеводород и отсутствие торможения при введении ингибитора в развившуюся реакцию. В начале реакции различие в активности радикалов из углеводорода и из ингибитора велико, и ингибитор тормозит окисление. В развивавшейся реакции радикалы, ведущие окисление, менее активны, разница в активности радикалов реакции и радикалов из ингибитора мала или вовсе отсутствует и торможения нет при введении ингибитора. Точно так же можно подойти к анализу кинетических закономерностей окисления смесей нескольких углеводородов. [39]
На рис. 1 представлены кинетические кривые расхода л-цимола во времени н накопления продуктов окисления. [40]
На рис. 1 представлены кинетические кривые расхода я-цимола во времени и накопления продуктов окисления. Из полученных данных видно, что основным продуктом окисления является п - ИПБК. [41]
Поэтому свободные радикалы RO2, ведущие цепь окисления, по мере накопления продуктов окисления во все возрастающей степени начинают взаимодействовать не с исходным углеводородом, а с продуктами окисления. Это может привести к существенным изменениям как скорости, так и направления процесса окисления. [42]
Схема эта почти не приобрела сторонников, так как последующее изучение кинетики накопления продуктов окисления парафиновых углеводородов показало, что соответствующие олефины не являются в этих случаях промежуточными веществами, поскольку их концентрация по ходу реакции не проходит через максимум. А именно это должно было бы быть согласно схеме Льюиса. [43]
 |
Кинетика поглощения кислорода полиэтиленом при 16Q C и различном содержании СН3 - групп на 1000 атомов С. [44] |
Продолжение окисления, сопровождающееся сшиванием макроцепей ( в основном кислородсодержащими мостиками) и накоплением труднокристаллизующихся продуктов окисления, приводит ко все большей аморфизации полиэтилена. [45]
Страницы: 1 2 3 4