Треххлористое железо
Cтраница 3
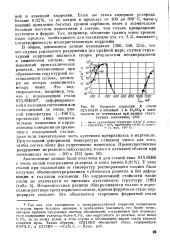 |
Скорость коррозии К стали. [31] |
У этих сталей при охлаждении от температур растворяющего отжига была получена объемноцентрированная кубическая решетка и без деформации в холодном состоянии. Незначительная разница обнаруживается только в агрессивном растворе треххлористого железа, причем ферритная сталь корродирует сильнее. [32]
При этом в качестве газовой фазы были использованы водород, аргон, фреон - 12, метан, азот, этилен, пропилен, гелий, пропан, углекислый газ. В этих опытах в качестве жидкостей были использованы: водные растворы соды, треххлористого железа, а также керосин, дитолилметан, октанол, терпениол, полиметилоксаны. [33]
Для полного разложения требуется температура 350е С. Однако в присутствии активированного угля, окислов алюминия и железа, хлористого олова, треххлористого железа и треххлористого алюминия разложение происходит уже при комнатной температуре. [34]
Для полного разложения требуется температура 350 С. Однако в присутствии активированного угли, окислов алюминия и железа, хлористого олова, треххлористого железа н трех хлористого алюминия разложение происходит уже при комнатной температуре. [35]
 |
Фильтрация. Снижение. [36] |
Губкина разработана рецептура раствора на нефтяной основе следующего состава: дизельное топливо, до 20 % глины или глинопорошка, до 3 % на сухое вещество в виде водного раствора 70 % - ной концентрации треххлористого железа ( РеС13), до 7 % сульфоолеина ( СТУ 7721 - 103 - 64) - поверхностно-активное вещество применяется в текстильной промышленности для окраски тканей, барит при необходимости. [37]
Обычно хлористый электролит имеет зеленый цвет. Пожелтение электролита свидетельствует о накоплении в нем треххлористого железа, что отрицательно сказывается на качестве осадка. Устранение треххлористого железа достигается добавлением в электролит железной стружки при последующей проработке ванн током. [38]
 |
Внешний вид спектрофотометра СФ-16. [39] |
В колбу вместимостью 100 мл помещают 0 2 0 0002 г испытуемой синтетической жирной кислоты, приливают 20 мл этилового спирта и после ее полного растворения приливают 5 мл водно-спиртового раствора солянокислого гидроксиламина, 6 мл спиртового раствора гидроксида калия и перемешивают. Через 5 - 10 мин приливают из бюретки водно-спиртовой раствор НС1 в объеме, определенном, как указано выше. К охлажденному раствору приливают 5 мл водно-спиртового раствора треххлористого железа и после перемешивания фильтруют его через бумажный фильтр в стакан вместимостью 50 мл. [40]
Предполагалось, что пленки ферромагнетиков на поверхности глинистых частиц удерживают углеводородные жидкости, снижая ц при вытеснении водой. Для проверки этой гипотезы были проведены следующие исследования. При обработке глины водным раствором НС1 гетит превращается в треххлористое железо, которое не обладает магнитными свойствами. [41]
Предполагалось, что пленки ферромагнетиков на поверхности глинистых частиц удерживают углеводородные жидкости, снижая г при вытеснении водой. Для проверки этой гипотезы были проведены следующие исследования. При обработке глины водным раствором НС1 гетит превращается в треххлористое железо, которое не обладает магнитными свойствами. [42]
Большую группу катализаторов алкилирования составляют ап-ротонные кислоты ( кислоты Льюиса) - галогениды некоторых металлов. Они обычно проявляют каталитическую активность в присутствии промоторов, с которыми образуют продукты, имеющие характер сильных протонных кислот. Из катализаторов этого типа могут применяться хлористый алюминий, бромистый алюминий, треххлористое железо, хлористый цинк, треххлористый и четырех-хлористый титан. Промышленное применение имеет только хлористый алюминий. [43]
Большую группу катализаторов алкилирования составляют апротонные кислоты ( кислоты Льюиса) - галогениды некоторых металлов. Они обычно проявляют каталитическую активность в присутствии промоторов, с которыми образуют продукты, имеющие характер сильных протонных кислот. Из катализаторов этого типа могут применяться хлористый алюминий, бромистый алюминий, треххлористое железо. Промышленное применение имеет только хлористый алюминий. [44]
Большой группой катализаторов алкилирования являются галогениды металлов, которые часто называют апротонными кислотами. Они обычно проявляют каталитическую активность в присутствии промоторов, с которыми образуют продукты кислотного характера. Из катализаторов этого типа чаще всего применяются следующие безводные галогениды [6, 18]: хлористый алюминий, бромистый алюминий, треххлористое железо, хлористый цинк, треххлористый титан и четыреххлористый титан. Сравнительно реже применяются для алкилирования четыреххлористое олово, четыреххлористый цирконий, пятихлористая сурьма, шестихлористый ванадий, двзгхлористая медь и другие галогениды. [45]
Страницы: 1 2 3 4