Наличие - компенсационный эффект
Cтраница 2
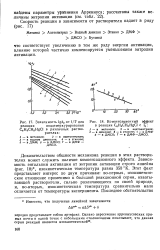 |
Зависимость lg. 2 от 1 / Т для реакции иоддемеркурирования.| Компенсационный эффект в реакции CeH5CH2HgCl с Ц. [16] |
Доказательством общности механизма реакции в этих растворителях может служить наличие компенсационного эффекта. Зависимость энтальпии активации от энтропии активации строго линейна ( рис. 18), изокинетическая температура равна 350 К. Этот факт представляет интерес по двум причинам: во-первых, изокинетиче-ское отношение применимо к большой реакционной серии, охватывающей растворители, сильно различающиеся по своей природе, и, во-вторых, изокинетическая температура сравнительно мало отличается от температуры эксперимента. [17]
Таким образом, следует весьма осторожно подходить к экспериментальным доказательствам наличия компенсационного эффекта. [18]
Значения h остаются достаточно постоянными в группах близких реакций ( см. табл. 1), что подтверждает наличие компенсационного эффекта. Существование последнего становится особенно очевидным при рассмотрении рис. 12 6, где представлены данные опытов, проведенных на одном и том же образце катализатора постоянной активности. Поэтому общая поверхность была строго постоянна. Точки хорошо ложатся на прямую, за исключением аллилового спирта; это неудивительно, если учесть особую структуру образующегося акролеина и изоамилового спирта. [19]
В некоторых работах интервал изменений величин энергии активации составлял всего несколько ккал / моль, поэтому выводы о наличии компенсационного эффекта в таких случаях вряд ли могут быть достаточно обоснованными. [20]
Неоднозначность между величиной энергии активации и скоростью реакции может быть также следствием явления компенсационного эффекта, выражаемого уравнением gA B - a E, где В и а - константы. Наличие компенсационного эффекта, видимо, можно считать установленным для ряда конкретных случаев. Однако его механизм и даже общность закономерности продолжают оставаться предметом дискуссии. [21]
Аррениуса должны пересечься в одной точке. Однако в тех случаях, когда отмечается наличие компенсационного эффекта, прямые в одной точке часто не пересекаются. [22]
Как видно из таблицы, константа скорости диспропорциониро-ванйя мало зависит от полярности растворителя. Это, очевидно, обусловлено не отсутствием взаимодействия с растворителем, а наличием компенсационного эффекта. [23]
Из полученных данных видно, что скорость взаимодействия увеличивается при переходе от бутилового спирта к этиловому, что естественно было связать с возрастанием протонодонорных свойств растворителя. Однако сопоставление активационных параметров этих реакций указывает на отсутствие какой-либо зависимости между энергией активации и реакционной способностью реагентов. При этом механизм реакции в исследованных спиртах не изменяется, о чем свидетельствует наличие компенсационного эффекта. Существующее различие в скоростях реакций присоединения, по-видимому, не обусловлено кислотными свойствами среды, что можно объяснить высокой активностью, а следовательно, малой селективностью к донорам протона карбаниона, возникающего в переходном состоянии. [24]
В указанных выше работах рассматривались реакции дегидрирования спиртов и циклопарафинов на металлических нанесенных катализаторах. При этом металл рассматривался как некий квазирадикал и постулировалось, что реакции имеют только одну лимитирующую стадию. При реализации этих постулатов и с учетом наличия компенсационного эффекта в ряде однотипных реакций на данном катализаторе получаем, что логарифмы скорости или константы скорости реакции пропорциональны делокализуемости электрона ( электронов), который ( которые) определяет скорости лимитирующей стадии. На рис. V.4 показана линейная зависимость энергии активации дегидрирования спиртов на различных металлических катализаторах от делокализуемости электрона у а-водород-ного атома спирта. [25]
Страницы: 1 2