Наложение - внешний ток
Cтраница 1
Наложение внешнего тока ( катодного или анодного) на такой редокси-электрод не может изменить до известного значения потенциала. [1]
Наложение внешнего тока ( катодного или анодного) на такой редокси-электрод не меняет направления протекания этих реакций, пока не достигнуто определенное значение потенциала. [2]
Если наложением внешнего тока газопровод заполяризован до равновесного потенциала растворения металла, то анодный ток прекращается и коррозия приостанавливается. Дальнейшее повышение защитного тока нецелесообразно. Устройства защиты, расставленные вдоль трассы газопровода, обеспечивают режим катодной поляризации в соответствии с критериями электрохимической защиты. [3]
При установившемся процессе самопроизвольного ( без наложения внешнего тока) растворения металла скорости анодной и катодной реакций одинаковы. Равенство скоростей анодной и катодной реакций определяет стационарный потенциал металла в данном электролите и установившуюся скорость растворения. Из условия стационарности следует, что торможение хотя бы одной из реакций приводит к замедлению коррозионного процесса. Поскольку коррозия является электрохимическим процессом, то целесообразно применять электрохимические способы торможения анодной или катодной реакции. Поэтому электрохимические методы снижения коррозии предусматривают смещение потенциала как в отрицательном, так и в положительном направлении от стационарного значения. [4]
При катодной защите от коррозии с наложением внешнего тока необходимый защитный ток вырабатывается преобразователями - так называемыми защитными установками. [6]
Для протекания коррозионного процесса совсем не обязательно наложение внешнего тока и тем не менее растворение металла в условиях коррозии совершается со скоростями, сравнимыми с теми, какие наблюдаются при растворении металлических анодов в промышленных электролизерах. Причины, вызывающие такие большие скорости растворения металлов без наложения внешнего анодного тока, лежат в особенностях самого коррозионного процесса. [7]
Процесс экстрагивной коррозии может наблюдаться как при наложении внешнего тока вследствие анодного растворения сплава, так и за счет тока, создаваемого окислительно-восстановительной системой, присутствующей в растворе. Явление экстрагивной коррозии может быть объяснено с помощью дифференциальных анодных кривых и поляризационных диаграмм ( фиг. [8]
Согласно вышеизложенному, механизм электрохимической защиты заключается в наложении внешнего тока, поляризующего катодные участки локальных элементов, на поверхности металла до потенциала неполяризованных анодных участков. [9]
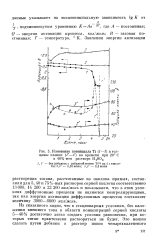 |
Изменение потенциала Ti ( 1 - 3 и толщины пленки (. - 3 во времени при 20 С в 40 % - ном растворе H2S04. [10] |
Из сказанного видно, что в стационарных условиях, без наложения внешнего тока в области концентраций серной кислоты 5 - 40 % достаточно легко создать условия равновесия, при которых титан практически растворяться не будет. [11]
В чистом 40 % - ном растворе серной кислоты в стационарных условиях без наложения внешнего тока наблюдается рост пленки на титане при потенциалах, близких - 0 4 в и ниже ( см. рис. 5), и по достижении максимальной толщины первичная окис-ная пленка растворяется. [12]
 |
Схема установки для снятия поляризационных кривых. [13] |
При 18 и 60 С в аэрированном растворе уксусной кислоты с добавкой муравьиной стали Х18Н10Т и ОХ21Н5Т легко поляризуются при наложении внешнего тока. [14]
 |
Схема установки для снятия поляризационных кривых. [15] |
Страницы: 1 2 3
