Жидкость - содовое производство
Cтраница 1
Жидкости содового производства являются смешанными растворами электролитов, которые включают разлагающиеся при нагревании компоненты. Перечисленные методы предназначены для ручного счета и непригодны для программирования на ЭВМ. [1]
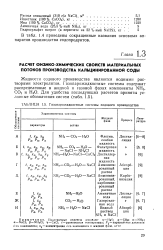 |
Газопарожидкостные системы содового производства. [2] |
Жидкости содового производства являются водными растворами электролитов. [3]
Плотность жидкостей содового производства рассчитывают методом коэффициентов [91, 92], принятым нами после анализа и прв лерки других рекомендуемых в литературе методик. [4]
В процессе дистилляции регенерируют аммиак из жидкостей содового производства и возвращают его на аммонизацию рассола. Дистилляции подвергают фильтровую жидкость, содержащую связанный ( в виде NH4C1 и небольшого количества ( NH4) 2S04) и полусвязанный аммиак ( в виде NH4OH, NH4HC03 и ( NH4) 2C03), а также слабые жидкости, получаемые, например, при промывке газов сушильных печей и содержащие в основном свободный и полусвязанный аммиак. Процесс осуществляется в подогревателях для разложения соединений полусвязанного аммиака, в смесителе для регенерации связанного аммиака известковым молоком и в дистиллере - для отгонки паром растворенного аммиака. [5]
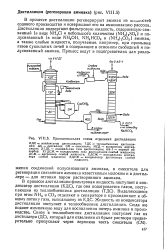 |
Принципиальная схема отделения дистилляции. [6] |
В процессе дистилляции регенерируют аммиак из жидкостей содового производства и возвращают его на аммонизацию рассола. [7]
В процессе дистилляции регенерируют аммиак из жидкостей содового производства и возвращают его на аммонизацию рассола. Дистилляции подвергают фильтровую жидкость, содержащую связанный ( в виде NH4C1 и небольшого количества ( NH4) 2S04) и полусвязанный аммиак ( в виде NH4OH, NH4HG03 и ( NH4) 2C03), а также слабые жидкости, получаемые, например, при промывке газов сушильных печей и содержащие в основном свободный и полусвязанный аммиак. Процесс осуществляется в подогревателях для разложения соединений полусвязанного аммиака, в смесителе для регенерации связанного аммиака известковым молоком и в дистиллере - для отгонки паром растворенного аммиака. [8]
В [3, 4] приведены методики расчета параметров различных физико-химических свойств жидкостей содового производства. Здановского, которое предполагает неизменность активности воды при смешении изоактивных растворов, компоненты которых не вступают в химическое взаимодействие. При наличии химического взаимодействия могут быть значительные отклонения от этого правила, особенно в области концентраций, близких к насыщению. В таких случаях следует применять либо иные математические модели, чем в [4], либо теории, способные описать свойства концентрированных растворов. [9]
В связи с этим были исследованы и усовершенствованы методы расчета параметров физических свойств жидкостей содового производства. Для аппроксимации параметров газо-парожидкостного равновесия были получены эмпирические формулы. Параметры физических свойств газов содового производства определяются известными методами, удобными для программирования на ЭВМ. Следует отметить, что при разработке указанных алгоритмов широко использовались литературные рекомендации, позволившие отобрать методики, которые предусматривают наименьший объем вычислительных операций и обеспечивают наибольшую точность вычислений. Зависимости, приведенные в литературе в табличной и графической форме, аппроксимированы аналитическими функциями и приведены к виду, удобному для использования на ЭВМ. В ряде случаев существующие методики были усовершенствованы. [10]
Исследованы также процессы десорбции аммиака из жидкостей содового и коксохимического производства, двуокиси углерода из жидкостей содового производства, бензольных углеводородов из каменноугольного масла. [11]
Методика расчета температуры кипения жидкостей, содержащих углеаммоншшые соединения, приведена выше, при этом более точное значение свободного члена соответствующих уравнений из табл. 5 можно получить по уравнению ( 33) с учетом только неразлагающихся при нагревании солевых компонентов. Поверхностное натяжение жидкостей содового производства вычисляется по методике, основанной на следующей закономерности [87] - поверхностное натяжение раствора электролита однозначно определяется величиной давления насыщенного пара воды над ним и не зависит от индивидуальных особенностей растворенных веществ. [12]
Хлористый барий может быть получен и другими способами, помимо рассмотренных выше. Представляет интерес способ получения хлористого бария обработкой BaS хлористым аммонием с использованием для этой цели решоферной жидкости содового производства. [13]
Производство соды по аммиачному способу является весьма несовершенным по степени использования сырья. Степень утилизации натрия составляет около 65 %, а хлор-ион совсем не утилизируется. Сброс хлоридов с жидкостями содового производства в реки недопустим. Поэтому в настоящее время внедряются в производство способы получения из жидкостей содового производства тукового хлористого аммония, хлористого кальция и пищевой поваренной соли. [14]
Система NaCl - СаС12 - Н20 представляет и теоретический и практический интерес. Она является типичным примером смешанных растворов сильных электролитов различного типа, и ее изучение позволяет расширить наши представления о влиянии электровалентности ионов на термодинамические свойства смешанных растворов. С практическим использованием данных о физико-химических свойствах таких растворов приходится сталкиваться в технологии получения СаС12 из отбросных жидкостей содового производства. [15]
Страницы: 1 2