Нарушение - условие - равновесие
Cтраница 3
 |
Иллюстрация к ста - И в этом случае статистика Больцмана тистике Бозе - Эйнштейна. применима при cof п т. е. уравне. [31] |
Таким образом, сог - п будет число ячеек, характеризующихся одинаковой скоростью реакции, так как теоретически допустимо введение катализатора, который обеспечит это без нарушения условий равновесия. [32]
 |
Открытия наиболее важных явлений электростатики. [33] |
Частицы и другие носители зарядов обеих полярностей распределены в материалах равномерно, поэтому вещество электрически нейтрально. Разрушение этого нейтрального состояния и локальное накопление униполярных частиц может привести к тому, что вещество станет заряженным. Это означает, что в основе электризации лежит нарушение условия равновесия зарядов. [34]
Это определение, конечно, не является строгим. Под виртуальной скоростью или перемещением следует понимать скорости или перемещения, совместимые со связями. Лагранж суживает определение, понимая под виртуальным перемещением или скоростью одно из действительных перемещений или скоростей, а именно то, которое произойдет при нарушении условий равновесия. [35]
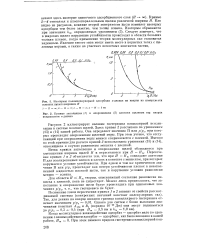 |
Изотермы полимолекулярной адсорбции к-декана на кварце на поверхности.| Кривые заполнения ( 1 и опорожнения ( 2 плоских щелевых пор кварца конденсатом к-декана. [36] |
Ветви кривых заполнения и опорожнения щелей сближаются при уменьшении ширины щелей Н и пересекаются при / / Нт. Пересечение кривых 1 т 2 объясняется тем, что при Н Нт совпадают значения П для изолированных пленок и пленок в контакте с мениском, при которых нарушается условие устойчивости. При одном и том же критическом значении П или p / ps происходит как потеря устойчивости пленок в незаполненной жидкостью плоской щели, так и нарушение условия равновесия мениск - пленка. [37]
Во всех процессах горения, независимо от их химической природы, основную роль играют критические явления и явления распространения зоны реакции. Критические явления характеризуются резким изменением режима протекания процесса при малом изменении внешних условий. Наиболее резко проявляется влияние температуры; было время, когда рассматривали температуру воспламенения как физическую константу горючей смеси и полагали, что при этой температуре скачком меняется скорость реакции. В действительности известно, что скорости всех элементарных химических процессов являются непрерывными функциями температуры; их температурная зависимость выражается законом Аррениуса. Критические явления происходят не от разрывного характера законов природы, а от нарушения условий равновесия между реагирующей системой и окружающей средой. [38]
Страницы: 1 2 3