Кривая жидкость
Cтраница 1
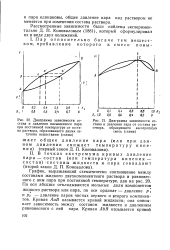
Кривые жидкости и пара в изученных системах не имеют экстремумов на диаграммах t - X, Y. Однако они располагаются ниже соответствующих кривых, рассчитанных в предположении об идеальности системы. [1]
 |
Диаграммы раствора. а - lj, (. б - ., г для одного давлении. [2] |
Меркелем, равновесные кривые жидкости и пара не совпадают, так как энтальпия пара выше энтальпи-л жидкости. [3]
На основании кривой жидкости и кривой пара ( рис. 132) строится кривая ABC, называемая кривой равновесия фаз. Каждая точка этой кривой отвечает особой температуре и показывает, каково содержание более летучего компонента в жидкой и газообразной фазах, находящихся в равновесии. [4]
Кривая АаВ называется кривой жидкости; она описывает зависимость между составом жидкости и давлением равновесного с ней пара. [6]
Вся область диаграммы выше кривой жидкости отвечает жидкому состоянию. Чем больше мы удаляемся вверх от оси абсцисс, тем выше давление, под которым находится жидкость. Если раствор под действием повышающегося давления начинает кристаллизоваться, то на диаграмме появляются соответствующие кривые. Этот вопрос будет рассмотрен ниже. [7]
Точка р лежит на кривой жидкости. При сжатии жидкой фазы, отвечающей точке р, появляется вторая фаза - пар; соотношение между количествами каждой из фаз определяется на основании ноды, проходящей через соответствующую фигуративную точку, например, на основании ноды п пъ проходящей через точку о. Пар, образовавшийся во время первых стадий сжатия, затем снова переходит в жидкое состояние, и когда объем системы сократится до величины, отвечающей точке q, система снова представляет собой одну жидкую фазу. Получившаяся жидкость сохраняет свое агрегатное состояние при дальнейшем увеличении давления. Процесс, при котором жидкость под влиянием возрастающего давления сначала частично переходит в пар, а образовавшийся пар затем снова переходит в жидкость, называется обратной конденсацией второго рода. [8]
Пусть точка L на изобарной равновесной кривой жидкости АС является фигуративной точкой жидкой начальной системы, находящейся при температуре кипения ( фиг. Состав а этой системы заключен в интервале концентрации U а ХА. [9]
 |
Применение правила касательной в случае. а - эвтектического равновесия. б - перитектического равновесия. в - перехода эвтектического равновесия в перитектичсское. [10] |
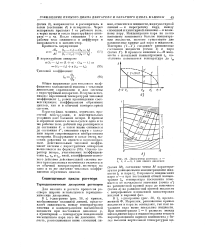
Так, если касательная к моновариантной кривой жидкости в интересующей нас точке проходит внутри стороны сф треугольника, как на рис. 178, я, имеет место эвтектическая кристаллизация. Если, наоборот, касательная к кривой жидкости проходит вне стороны оф, как на рис. 178 6, имеет место перитектическая кристаллизация. То обстоятельство, что в этом последнем случае касательная пересекается с продолжением стороны оф, следует истолковать таким образом, что выделяющаяся из жидкости смесь не может в этом случае состоять из а - и В-кристаллов, но может образовать а-кристаллы за счет превращения В-кристаллов. [11]
Рассмотрим более подробно некоторые особенности граничных кривых жидкости и газа. Форма граничной кривой жидкости AD / C на рис. 3 дает представление о зависимости растворимости метана в декане от давления. При давлениях до 30 кгс / см2 приближенно соблюдается прямая пропорциональность. [12]
Критическая точка D соответствует месту соединения кривых жидкости и пара. [13]
 |
К объяснению Коновалова. [14] |
На диаграммах это изображается тем, что кривые жидкости и пара сливаются, поэтому для экстремальных точек ху. Отсюда следует, что смеси, имеющие максимальную или минимальную температуры кипения, нельзя разделить перегонкой. Перегонка всегда приводит к составу, имеющему экстремальную температуру кипения. [15]
Страницы: 1 2 3 4 5