Водородистый натрий
Cтраница 2
Для измерения упругости диссоциации применялся описанный выше прибор и только ампула, в которой помещался металлический натрий, имела в данном случае специальную форму. Дело в том, что при первых же ориентировочных опытах было замечено, что водородистый натрий образует белые волокнистые кристаллы, которые возгоняются и закупоривают капилляр в месте припая его к ампуле, в которую помещался натрий. [16]
Очистку проводят в ваннах, заполненных каустической содой и металлическим натрием, который при рабочей температуре находится на поверхности в виде жидкого слоя ( фиг. Под слой расплавленного натрия по трубочкам в ванну подается водород, вступающий при соприкосновении с натрием в реакцию с образованием водородистого натрия. [17]
Из того, что полученный ими продукт имел металлический вид и обладал способностью поглощать водород иод давлением, они заключают, что натрий поглощает водород подобно палладию и образует сплав с водородом. Троост и Готфейль не исследовали упругости диссоциации в зависимости от количества поглощенного натрием водорода и потому на основании их данных нельзя сделать какого-либо определенного вывода относительно природы описываемого ими водородистого натрия. [18]
 |
Схема установки ( электролизера для пол чения металлического натрия электрохимическим путем.| Схема образования отрицательно одновалентного иона водорода. [19] |
Водородистый натрий - твердое, белое вещество; легко разлагается водой. [20]
Окалина хорошо удаляется с поверхности изделий водородистым натрием при температуре 350 - 370 С. Водородистый натрий является сильным восстановителем, вступая в реакцию со многими окислами металлов он совершенно не действует на металл, находящийся под окисной пленкой. [21]
Трост и Готфейль в 1874 г. заметили, что натрий, вовсе не реагирующий с водородом при обыкновенной температуре, поглощает водород ( 238 объемов на 1 объем Na) при температурах 300 - 420; объем металла увеличивается и при охлаждении водород не выделяется, но при температуре выше 320 происходит диссоциация. Очевидно, что из натрия при этом образуется водородистый натрий, но в чистом виде это вещество получено только Муассаном в 1902 г., когда он вложил металлический натрий в железную трубку, нагретую снизу до 360, а сверху имеющую низшую температуру, и пропускал чрез нее сухой водород. При этом образовавшийся водородистый натрий NaH осаждается на верхних частях трубки в виде бесцветного кристаллического возгона. Полученный этим путем NaH прямо окисляется на воздухе, тотчас и сильно реагирует с хлором, кислородом ( горит в нем) и многими другими газами и жидкостями. [22]
В 1874 г. Троост и Готфейль [1.1] опубликовали работу, в которой описали свойства полученных ими водородистых натрия и калия. Согласно их данным, металлический натрий начинает поглощать водород при 300, но при этой температуре поглощение идет медленно. С повышением температуры скорость поглощения увеличивается, и 350 представляют собою оптимум для образования водородистого натрия. При этом получается мягкий, серебристого цвета продукт, который плавится ниже температуры плавления чистого натрия и около своей температуры плавления становится кристалличтшм и хрупким. [23]
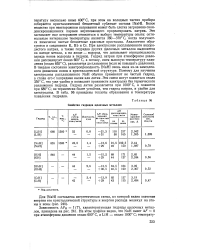 |
Свойства гидридов щелочных металлов. [24] |
Белое вещество при неосторожном нагревании может быть слегка загрязнено сконденсировавшимися парами неуспевающего прореагировать натрия. Это заставляет еще осторожнее относиться к выбору температуры опыта: оптимальным интервалом температуры является 360 - 370 С, когда получаются химически чистые бесцветные красивые кристаллы. Аналогично образуются и соединения К, Rb и Cs. При электролизе расплавленного водородистого натрия, а также гидридов других щелочных металлов выделяется на катоде металл, а на аноде - водород, что доказывает отрицательность заряда ионов водорода в гидриде. В твердом состоянии электропроводность [ NaH ] очень мала из-за замедленного движения ионов в кристаллической структуре. Поэтому для изучения электролиза расплавленного NaH обычно применяют не чистый гидрид, а сплав его с хлоридами калия или лития. Эти смеси могут плавиться около 350 С, что уже удобно и позволяет произвести электролиз без термического разложения гидрида. Гидрид лития разлагается при 1000 С, а плавится при 680 С; он термически более устойчив, чем гидрид натрия, и удобен для электролиза. В табл. 96 приведены теплоты образования и температуры плавления гидридов. [25]
XX Y, а двуатомные Y, иногда могущие существовать отдельно, соединяются между собою YY и с X2 или с XX, как и видим при переходе СО в СО2 и в СОСГ2 - Эта способность окиси углерода к соединениям проявляется во многих ее реакциях. Мондом ( описывается в главе 22), и, во-вторых, соединения СО со щелочами, напр. СО прямо не поглощается ими, так как не имеет кислых свойств. Вертело указал ( 1861), что едкое кали в присутствии воды способно поглощать окись углерода, но только такое поглощение происходит медленно, мало-помалу, и только по прошествии многих часов нагревания вся окись углерода поглощается едким кали. В образовании муравьиной кислоты из окиси углерода видим пример синтеза органических соединений, для которого ныне имеется множество примеров, подробнее разбираемых в органической химии. Муассан ( 1901) воспроизвел этот же синтез при помощи СО2, так как показал, что водородистый натрий NaH ( гл. [26]
Страницы: 1 2