Кислый углекислый натрий
Cтраница 1
Кислый углекислый натрий, или двууглекислая сода ( natrium bicarbonicum), NaHCO3 применяется как в виде cyxoft соли, так и в минеральных водах при хронических болезнях желудка, изжоге, подагре, диабете, катаррах верхних дыхательных путей, а также для ингаляций и полосканий. [1]
Кислый углекислый натрий NaHC03 ( сода питьевая или чайная) используется в кондитерском деле ( вместо дрожжей), в медицине и лабораторной практике. [2]
Кислый углекислый натрий, или двууглекислая сода ( natrium bicarbonicum), NaHCO3 применяется как в виде сухой соли, так и в минеральных водах при хронических болезнях желудка, изжоге, подагре, диабете, катаррах верхних дыхательных путей, а также для ингаляций и полосканий. [3]
Кислый углекислый натрий NaHC03 ( сода питьевая или чайная) используется в кондитерском деле ( вместо дрожжей), в медицине и лабораторной практике. [4]
В разбавленном растворе кислого углекислого натрия растворимы все сильнокислые вещества, например карбоновые кислоты. В разбавленной щелочи растворяются фенолы, первичные и вторичные нитросоединения, арилсульфонильные производные первичных аминов. [5]
В разбавленном растворе кислого углекислого натрия растворимы все сильнокислые вещества, например карболовые кислоты. [6]
В результате реакции образуется кислый углекислый натрий в количестве, эквивалентном 25 мл 0 1 М раствора; из 100 мл 0, 1 М раствора углекислого натрия не прореагирует 75 мл. Кислый углекислый натрий следует считать кислотой по отношению к углекислому натрию. [7]
В результате реакции образуется кислый углекислый натрий в количестве. Кислый углекислый натрий следует считать кислотой по отношению к углекислому натрию. [8]
В качестве противоядия принимают внутрь кислый углекислый натрий. [9]
Смесь угольной кислоты и кислого углекислого натрия также имеет свойства буферного раствора, причем теперь NaHCO3 играет роль соли по отношению к Н2С03, как кислоте. [10]
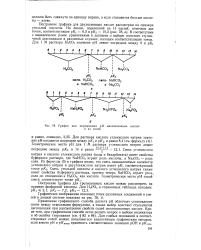 |
График для определения рН многоосновных кислот. [11] |
Смесь углекислого натрия и кислого углекислого натрия ( соды и бикарбоната) имеет свойства буферного раствора, где NaHCO3 играет роль кислоты, a Na2CO3 - роль соли. Из формулы ( 3) и графика видно, что смесь эквивалентных количеств углекислого натрия и двууглекислого натрия имеет рН, соответствующий точке pKz - Смесь угольной кислоты и кислого углекислого натрия также имеет свойства буферного раствора, причем теперь NaHCO3 играет роль соли по отношению к Н2СО3, как кислоте. [12]
Угольная кислота вместе с кислым углекислым натрием и калием образует так называемую буферную систему, которая с другими буферными системами крови обладает способностью противодействовать изменению концентрации водородных ионов при появлении в организме тех или иных свободных кислот или оснований. [13]
На этой реакции основано применение кислого углекислого натрия в твердом состоянии для тушения пламени легких металлов и других веществ, а также газов, выделяющихся под давлением из трубопроводов и газохранилищ. Твердый NaHCO3 выбрасывают под давлением из специальных переносных приборов или постоянно действующих установок. Образующиеся при нагревании NaHCO, двуокись углерода и водяной пар изолируют пламя от воздуха. [14]
Для титрования углекислого натрия до кислого углекислого натрия обычно применяют в качестве индикатора фенолфталеин, а при титровании до угольной кислоты - метилоранжевый; последнее титрование дает более точные результаты. [15]
Страницы: 1 2 3