Неограниченно растворимая жидкость
Cтраница 1
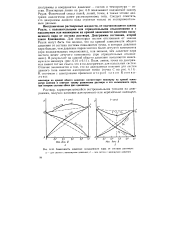 |
Зависимость давления насыщенного пара от состава раствора. а - для систем с максимумом давления. 6 - для систем с минимумом давления. [1] |
Неограниченно растворимые жидкости, не подчиняющиеся закону Рауля, с положительными или отрицательными отклонениями и с максимумом или минимумом на кривой зависимости давления насыщенного пара от состава раствора. Диаграммы состояния, второй закон Коновалова. Поля, линии, точки на диаграммах имеют тот же смысл, что и на диаграммах для идеальных систем. [2]
Неограниченно растворимые жидкости, подчиняющиеся закону Рауля. [3]
Этот закон справедлив для всех типов неограниченно растворимых жидкостей. Математически неравенство составов равновесных фаз можно обосновать следующим образом. Вполне очевидно, что при данной температуре пар обогащен более летучим компонентом В. [4]
Системы, состоящие из двух и более неограниченно растворимых жидкостей, имеют важное практическое значение. Такие системы наблюдаются в технологических процессах ректификации, экстракции и др. Зависимость некоторых свойств систем от их состава изучают с помощью диаграмм состояния: давление насыщенного пара - состав, температура кипения - - состав. Диаграммы состояния наглядно показывают, что происходит в системах при нагревании, охлаждении и изменении их состава. [5]
В производственных условиях довольно часто приходится иметь дело со смесями двух неограниченно растворимых жидкостей. Знание закономерностей испарения таких систем позволяет осуществлять разделение их на составные части. [6]
На различии в равновесных составах жидкой и паровой фаз основано разделение неограниченно растворимых жидкостей перегонкой. На диаграмме кипения верхняя линия t fu выражает зависимость температуры конденсации пара от его состава. Нижняя линия А / в выражает зависимость температуры кипения раствора от его состава. Диаграмма двумя линиями разделена на три поля. Каждой температуре кипения соответствуют определенные составы жидкой и паровой фаз. Любая фигуративная точка в поле 3 ( например, точка а) отражает валовый ( общий) состав системы. Чтобы найти составы фаз, необходимо провести изотерму через точку а. Пар обогащен компонентом В. [7]
По характеру зависимости давления насыщенных паров от состава раствора при постоянной температуре неограниченно растворимые жидкости разделяют на три типа: 1) идеальные, подчиняющиеся закону Рауля; 2) с положительными или отрицательными отклонениями от закона Рауля, но без максимума или минимума на кривой зависимости давления насыщенного пара от состава раствора; 3) с максимумом или минимумом на кривой зависимости давления насыщенного пара от состава раствора. [8]
Киселев и Павлова [75] рассмотрели полное изменение энергии Гиббса при изотермической адсорбции двух взаимно неограниченно растворимых жидкостей на химически и геометрически однородной твердой поверхности. [9]
Киселев и Павлова [75] рассмотрели полное изменение энергии Гиббса при изотермической адсорбции двух взаимно неограниченно растворимых жидкостей на химически и геометрически однородной твердой поверхности. [10]
Одновременно происходит изменение соотношения масс фаз. По мере кипения жидкость испаряется и ее количество уменьшается. Согласно правилу рычага ( см. § 6.2), пунктирные линии характеризуют массу жидкой фазы, сплошные линии - массу паровой фазы. Неограниченно растворимые жидкости, не подчиняющиеся закону Рауля, с положительными или отрицательными отклонениями, но без максимума или минимума на кривой зависимости давления насыщенного пара от состава раствора. Образование растворов с положительными отклонениями сопровождается поглощением теплоты, что облегчает испарение. [11]
Страницы: 1