Недостаток - электрон
Cтраница 3
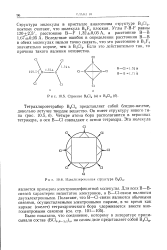 |
Строение В2С14 ( а и В4С14 ( б. [31] |
Для всех В-В - связей характерен недостаток электронов, а В - С1 - связи являются двухэлектронными. Полагают, что В-Cl - связи являются обычными связями, осуществляемыми электронными парами, в то время как каркас ( скелет) тетраэдрического бора удерживается вместе многоцентровыми связями ( см. стр. [32]
Здесь знак Q над М означает недостаток электронов. Гидроксильные радикалы, образованные на поверхности, попарно реагируют с образованием молекулярного кислорода, причем промежуточная стадия или промежуточные стадии протекают относительно быстро. [33]
С-атомов 2 4 и 6 наблюдается недостаток электронов. Поэтому реакции электрофильного замещения в пиридине протекают только в положении 3 ( мета -) и притом относительно трудно. [34]
Поскольку стремление электроположительного атома углерода восполнять недостаток электронов больше, чем стремление электроотрицательного атома азота отдавать избыток электронов, нитрилы обладают преимущественно электрофильной реакционной способностью. Однако в CN-rpynne имеются неподеленная электронная пара, а также электронодонорные я-связи, поэтому нитрилы проявляют и нуклеофильные свойства. [35]
Так как в рассматриваемых случаях имеется недостаток электронов как в ВН3, так и в реагирующих с ним веществах, - атомы, стремясь создать по возможности заполненные электронами оболочки, принимают участие в построении своеобразных продуктов присоединения - двойных гидранов так называемых боранатов. [36]
Для всех В-В - связей характерен недостаток электронов, а В - С1 - связи являются двухэлектронными. Полагают, что В - С1 - связи являются обычными связями, осуществляемыми электронными парами, в то время как каркас ( скелет) тетраэдрического бора удерживается вместе многоцентровыми связями ( см. стр. [37]
К электронным дефектам относятся избыточные электроны, недостаток электронов ( дырки) и экситоны. Последние представляют собой парные дефекты, состоящие из электрона и дырки, которые связаны кулоновскими силами. [38]
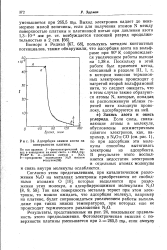 |
Адсорбция закиси азота на поверхности платины. [39] |
В результате этого воспол - - няется недостаток электронов в отдельных атомах молекулы и связь внутри молекулы ослабляется. [40]
Электрофильные свойства определяет не заряд, а недостаток электронов. [41]
К электронным дефектам относятся избыточные электроны, недостаток электронов ( дырки) и экситоны. Последние представляют собой парные дефекты, состоящие из электрона и дырки, которые связаны кулоновскими силами. [42]
Электрофильные свойства определяет не заряд, а недостаток электронов. [43]
К электронным дефектам относятся избыточные электроны, недостаток электронов ( незаполненные валентные связи в кристалле - дырки) и экситоны. Последние представляют собой парные дефекты, состоящие из электрона и дырки, которые связаны кулоновскими силами. Более подробно этот вопрос изложен в гл. [44]
Электрофильные свойства определяет не заряд, а недостаток электронов. [45]
Страницы: 1 2 3 4