Неидеальность - система
Cтраница 1
Неидеальность систем с химически не взаимодействующими компонентами приводит к большим относительным отклонениям от аддитивности, чем это наблюдается в случае иных объемно-аддитивных свойств - плотности и показателя преломления. Во всех случаях, где удалось провести сопоставление, изотермы интегральной интенсивности В характеризуются меньшими величинами /, чем изотермы оптической плотности. [1]
Степень неидеальности систем, включающих полярный растворитель и углеводороды различных гомологических рядов ( при одинаковом числе углеродных атомов в молекулах), изменяется, как правило, в следующем ряду углеводородов [21, 22]: алка-ны циклоалканы ж алкены алкадиены алкины ал-килбензолы алкилнафталины. В этой же последовательности при переходе от алканов к аренам возрастают значения силовых полей и параметров растворимости [23] молекул углеводородов, а также силы притяжения к молекулам полярных растворителей. [2]
Степень неидеальности системы определяется различием химической природы и строения молекул компонентов. На основании изложенных выше представлений о природе межмолекулярного взаимодействия и роли химических и структурных факторов, представляется возможным качественно предсказать степень неидеальности бинарной системы. Количественно ее можно оценить, используя данные, позволяющие рассчитать коэффициент активности хотя бы одного компонента. [3]
Для характеристики неидеальности системы по отношению к растворителю часто предпочтительнее вместо коэффициента активности использовать осмотический коэффициент ф Бьеррума и Гутгенгейма. [4]
С увеличением степени неидеальности системы возрастает интервал изменения отношения коэффициентов активности компонентов при изменении состава. При этом могут удовлетворяться и условия образования конгруэнтно испаряющегося раствора, выражаемые уравнениями ( IV-371) или ( IV-372), и условие образования азеотропной смеси ( у ] / у2 РУР) - Оба условия могут удовлетворяться одновременно при таком составе твердой фазы, при котором ее термодинамические свойства, в том числе величина y2 / Yi изменяются скачкообразно. [5]
Обнаружение отказа задерживается из-за неидеальности системы контроля работоспособности. При периодическом контроле интервал времени необнаруженного ( скрытого) отказа исчисляется от момента возникновения отказа до ближайшей контрольной проверки. Между соседними проверками обесценивается и часть полезной работы, выполненной за время от начала этапа до момента отказа. Скрытые отказы могут возникать и при непрерывном, но неполном контроле. В этом случае в аппаратуре, не охваченной автоматическим контролем, отказы обнаруживают по косвенным признакам и часто с существенной задержкой. В ЦВМ задержки вызваны ошибками в исходных данных, подготавливаемых за ее пределами, а в производственных системах - браком, обнаруживаемым лишь при выходном контроле качества продукции. [6]
Михайлов [15] нашел, что неидеальность систем дибутилфосфорная кислота - разбавитель ( СвНв, СС14, СНС13, гептан) близка к наблюдаемой в системах с ТБФ. Вероятно, это связано с возрастанием положительной неидеальности вследствие полимеризации ДБФ с образованием тримеров или тетрамеров. [7]
А - коэффициент, являющийся мерой неидеальности системы. Образование азеотропа и его состав могут быть предсказаны по этому уравнению, если по каким-либо данным известен или может быть найден коэффициент А. [8]
Анализ результатов показывает, что средние по неидеальности системы описываются всеми пятью уравнениями приблизительно с равным успехом. В случае сильно неидеальных систем очевидно преимущество уравнений Вильсона и NRTL. Несмотря на низкий средний уровень корреляции данных с помощью уравнения UNIQUAQ имеются несколько подгрупп систем, где оно может конкурировать с другими уравнениями. [9]
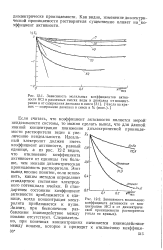
Если считать, что коэффициент активности является мерой неидеальности системы, то можно сделать вывод, что для данной ионной концентрации понижение диэлектрической проницаемости растворителя ведет к увеличению неидеальности. Идеальный электролит должен иметь коэффициент активности, равный D8 единице, а из рис. 12 - 2 видно, что отклонение коэффициента активности от единицы тем больше, чем меньше диэлектрическая проницаемость растворителя. Этот вывод вполне понятен, если вспомнить, каким методом определяют стандартное состояние электродного потенциала ячейки. В стандартном состоянии коэффициент активности приближается к единице, когда концентрация электролита приближается к нулю. [11]
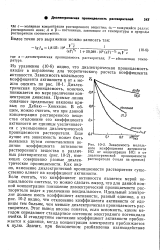 |
Зависимость моляльного коэффициента активности НС1 от концентрации НС1 и от. [12] |
Если считать, что коэффициент активности является мерой неидеальности системы, то можно сделать вывод, что для данной ионной концентрации понижение диэлектрической проницаемости растворителя ведет к увеличению неидеальности. Идеальный электролит должен иметь коэффициент активности, равный единице, а из рис. 10 - 2 видно, что отклонение коэффициента активности от единицы тем больше, чем меньше диэлектрическая проницаемость растворителя. Этот вывод вполне понятен, если вспомнить, каким методом определяют стандартное состояние электродного потенциала ячейки. В стандартном состоянии коэффициент активности приближается к единице, когда концентрация электролита приближается нулю. Значит, при бесконечном разбавлении взаимодействие. [13]
При расчете равновесных составов, вообще говоря, нужно учитывать неидеальность системы. Однако при умеренных давлениях, обычно применяемых для синтеза ( до 5 МПа), летучести компонентов близки к парциальным давлениям и предположение об идеальности системы не вносит заметной ошибки в расчеты. [14]
Было показано, что чем меньше растворимость, тем выше неидеальность системы. [15]
Страницы: 1 2 3 4