Нейтрализация - ион - водород
Cтраница 1
Нейтрализация ионов водорода и повышение температуры смещают равновесие вправо, добавление кислот ( особенно соляной) - влево. [1]
Рипан, после нейтрализации ионов водорода, отвечающих сильной кислотности. [2]
Ринан, после нейтрализации ионов водорода, отвечающих сильной кислотности. [3]
Для полноты протекания реакции необходима нейтрализация ионов водорода. Прибавление сильной щелочи недопустимо, так как она может вызвать осаждение гидроокиси марганца и способствовать частичному окислению ее кислородом воздуха. [4]
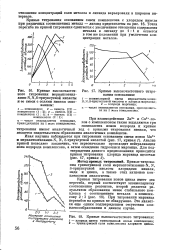
Уменьшение электропроводности при добавлении первых порций щелочи соответствует нейтрализации ионов водорода, присутствующих в исходном растворе кислоты. Однако в исходном растворе кислоты имеется лишь немного ионов водорода. [5]
Анализ кривой позволяет заключить, что первоначально происходит нейтрализация иона водорода комплексона, а затем осаждение гидроокиси марганца. [7]
Нам, однако, представляется маловероятным, чтобы при нейтрализации ионов водорода в растворе могла оставаться неионизированная сульфиновая кислота. [8]
Нам, однако, представляется маловероятным, чтобы при нейтрализации ионов водорода в растворе могла оставаться неионизированная сульфиновая кислота. [9]
Таким образом, ионы бикарбоната, использованные ранее для нейтрализации ионов водорода, восполняются, а моча закис-ляется. [10]
До сих пор было описано определение катионов, основанное на нейтрализации ионов водорода, выделяющихся при образовании комплексных соединений, или на изменении рН в процессе титрования раствором комплексона. [11]
По аналогии можно предположить, что вообще взаимная нейтрализация сильных оснований и кислот состоит в нейтрализации ионов водорода и гидроксила, а следовательно, тепловой эффект всех подобных реакций должен быть одинаков. [12]
Электрон, отрываемый от молекулы воды во время акта ионизации, уносит с собой некоторую значительную энергию, и часть таких электронов способна, в свою очередь, ионизировать и возбуждать молекулы воды. Возбужденная молекула воды также получается при нейтрализации ионов водорода частью более медленных электронов, причем сумма энергии нейтрализации иона Н30 и собственная энергия электрона превращаются в энергию возбуждения воды. [13]
Одним из эффективных методов очистки сточных вод от ПАВ, и прежде всего от анионных ПАВ, является обработка воды коагулянтами - солями алюминия или железа. При гидролизе этих солей в условиях нейтрализации ионов водорода бикарбонатами, растворенными в воде, либо известью образуются рыхлые хлопья гидрогеля гидроксидов алюминия или железа, обладающие крупнопористой структурой. [14]
Приготавливают в мерной колбе исходный раствор. Электропроводность раствора при титровании сначала немного понижается, что объясняется нейтрализацией высокоподвижных ионов водорода, образующихся при диссоциации титруемой кислоты. Однако образующаяся в процессе нейтрализации соль вызывает повышение электропроводности раствора. Поэтому кривая титрования имеет неглубокий минимум в начале титрования. После минимума электропроводность раствора линейно увеличивается до точки эквивалентности. При добавлении избытка аммиака электропроводность не изменяется. Кривая титрования имеет резкий излом в точке эквивалентности. [15]
Страницы: 1 2